题目内容
【题目】某酸性燃料电池(以甲醇为燃料,酸性介质)结构示意如图。下列有关说法正确的是
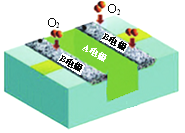
A. 电池工作时,电子由A电极经外电路流向B电极
B. 电池工作时,减少的化学能完全转化为电能
C. A电极发生的电极反应为:CH3OH-6e-+H2O=CO2+6H+
D. B电极每消耗1 mol O2,电池中减少4 mol H+
【答案】AC
【解析】根据示意图,B电极为正极,A电极为负极。A. 原电池中,电子由负极A经外电路流向正极B,故A正确;B. 电池工作时,主要是化学能转化为电能,但也有其他形式的能量变化,如热能,故B错误;C. A电极发生氧化反应,发生的电极反应为:CH3OH-6e-+H2O=CO2+6H+,故C正确;D. 根据总反应为甲醇与氧气反应生成二氧化碳和水,电池中的H+总量不变,故D错误;故选AC。
点晴:本题以甲醇为燃料考查了燃料电池,注意正负极上电极反应式的书写要结合电解质溶液的酸碱性,即使燃料和氧化剂相同,如果电解质溶液不同,电极反应式也不同。

 互动英语系列答案
互动英语系列答案【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
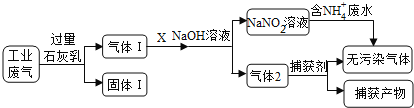
(1)固体I中主要成分为__________,捕获剂所捕获的气体主要是_________。
(2)处理含NH4+废水时,发生反应的离子方程式为___________。
(3)若X为适量空气,严格控制空气用量的原因是____________。
(4)工业废气中的SO2、NO还可采用NaClO2溶液作为吸收剂进行净化,在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表:
离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
c(mol·L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式_________________。
增加压强,NO的转化率__________(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐__________(填“增大”、“不变”或“减小”)。
③如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是_______________。
【题目】室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
实验编号 | 起始浓度/mol·L-1 | 反应后溶液的PH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | X | 0.2 | 7 |
下列判断不正确的是
A. 实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B. 实验①反应后的溶液中:c(OH-)= c(K+)-c(A_)=![]() mol·L-1
mol·L-1
C. 实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D. 实验②反应后的溶液中:c(K+)=c(A-)> c(OH-)=c(H+)