题目内容
【题目】下列有关平衡常数K的说法正确的是
A. 已知碳酸: K1=4.4×10-7,K2=4.7×10-11,次氯酸: K1=2.98×10-8,碳酸钠溶液中滴加少量氯水的离子方程式为: CO32-+Cl2+H2O=HCO3-+Cl-+HClO
B. 1.0mol/LNH4HCO3溶液pH=8.0。由此可知Ka1(H2CO3)> Kb(NH3·H2O)>Ka2(H2CO3)
C. 常温下电离常数为Ka 的酸HA溶液中c(H+)= ![]()
D. 将0.1mol/LMgSO4溶液滴入NaOH 溶液中至不再有沉淀产生,再滴加0.1mo/LCuSO4溶液,白色沉淀变为蓝色沉淀,可得出Ksp[Cu(OH)2]sp[Mg(OH)2]
【答案】D
【解析】已知碳酸:K1=4.4×10-7,K2=4.7×10-11,次氯酸:K1=2.98×10-8,碳酸钠溶液中滴加少量氯水的离子方程式为:2CO32-+Cl2+H2O=2HCO3-+Cl-+ClO-,故A错误;越弱越水解,1.0mol/LNH4HCO3溶液pH=8.0。由此可知Kb(NH3·H2O)>Ka1(H2CO3)> Ka2(H2CO3),故B错误;常温下电离常数为Ka的酸HA溶液中c(H+)= ![]() ,故C错误;一种沉淀容易转化为比它更难溶的沉淀,将0.1mol/LMgSO4溶液滴入NaOH溶液中至不再有沉淀产生,再滴加0.1mo/LCuSO4溶液,白色沉淀变为蓝色沉淀,可得出Ksp[Cu(OH)2]<Ksp[Mg(OH)2],故D正确。
,故C错误;一种沉淀容易转化为比它更难溶的沉淀,将0.1mol/LMgSO4溶液滴入NaOH溶液中至不再有沉淀产生,再滴加0.1mo/LCuSO4溶液,白色沉淀变为蓝色沉淀,可得出Ksp[Cu(OH)2]<Ksp[Mg(OH)2],故D正确。

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案【题目】某实验小组设计实验,利用酸性KMnO4溶液与H2C2O4溶液反应,测定溶液紫色消失所需时间的方法,研究浓度对反应速率的影响。供选择的实验药品有:0.01mol·L-1酸性KMnO4溶液、0.1mol·L-1酸性KMnO4溶液、0.1mol·L-1H2C2O4溶液、0.2mol·L-1H2C2O4溶液。
(1)H2C2O4溶液与酸性KMnO4溶液反应的化学方程式为____________________________。
(2)请完成以下实验设计表。
实验 | 酸性KMnO4溶液 | H2C2O4溶液 | 褪色 时间/s | ||
c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
甲 | 0.01 | 4 | 0.1 | 2 | t1 |
乙 | a | 4 | b | 2 | t2 |
①表中a=________、b=________;
②甲组实验KMnO4的平均反应速率是:____________(用含t1的式子表示)。
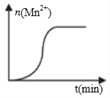
(3)测得某次实验(恒温)时,溶液中Mn2+物质的量与时间关系如图。请解释n(Mn2+)在反应起始时变化不大、一段时间后快速增大的原因:______。