题目内容
某化学兴趣小组用只含有铝、铁、铜的工业废料制取纯净的氯化铝溶液、绿矾晶体[FeSO4?7H2O]和胆矾晶体,以探索工业废料的再利用.其实验方案如下:
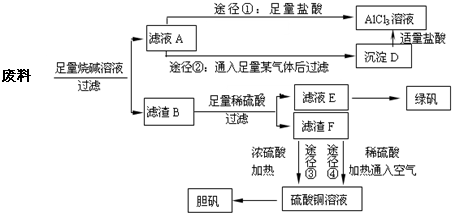
回答下列问题:
(1)写出合金与烧碱溶液反应的离子方程式
(2)由滤液A制AlCl3溶液的途径有①和②两种,途径②中通入的某气体其固态可用于人工降雨,则该气体是
(3)滤液E若放置在空气中一段时间后,溶液中的阳离子除了Fe2+和H+外,还最可能存在的阳离子是
(4)用滤渣F通过两种途径制取胆矾,与途径③相比,途径④明显具有的两个优点是
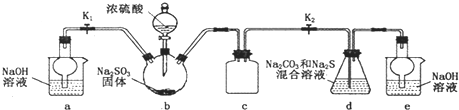
(5)途径③发生的反应中,体现了浓硫酸

回答下列问题:
(1)写出合金与烧碱溶液反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
.(2)由滤液A制AlCl3溶液的途径有①和②两种,途径②中通入的某气体其固态可用于人工降雨,则该气体是
CO2
CO2
(填化学式),滤液A与过量的某气体生成沉淀D的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
.你认为较合理的途径是②
②
(填①或②),理由是途径①会引入盐酸,氯化钠杂质
途径①会引入盐酸,氯化钠杂质
.(3)滤液E若放置在空气中一段时间后,溶液中的阳离子除了Fe2+和H+外,还最可能存在的阳离子是
Fe3+
Fe3+
(用离子符号表示),检测该离子的方法是取滤液E少量于试管中,滴入2~3滴KSCN溶液,若出现血红色,则证明滤液E中含有Fe3+
取滤液E少量于试管中,滴入2~3滴KSCN溶液,若出现血红色,则证明滤液E中含有Fe3+
.(4)用滤渣F通过两种途径制取胆矾,与途径③相比,途径④明显具有的两个优点是
产生等量胆矾途径④消耗硫酸少
产生等量胆矾途径④消耗硫酸少
、途径④不会产生污染大气的气体
途径④不会产生污染大气的气体
.(5)途径③发生的反应中,体现了浓硫酸
强氧化
强氧化
性和酸
酸
性.通过途径④制取胆矾,必须进行的实验操作步骤:加硫酸、加热通氧气、过滤、蒸发浓缩、冷却结晶、过滤
过滤
、自然干燥.其中途径④发生的反应为2Cu+O2+4H+=2Cu2++2H2O
2Cu+O2+4H+=2Cu2++2H2O
(用一个离子方程式表示).分析:(1)根据铝与碱反应生成偏铝酸钠和氢气;
(2)根据物质的性质结合框图转化关系和所得产品进行解答;
(3)二价铁易被空气中的氧气氧化成三价铁离子,检验三价铁离子用KSCN溶液;
(4)从环保和原料的利用率角度解答;
(5)铜与浓硫酸反应体现了浓硫酸的强氧化性和酸性,铜和氧气和酸反应生成铜离子;
(2)根据物质的性质结合框图转化关系和所得产品进行解答;
(3)二价铁易被空气中的氧气氧化成三价铁离子,检验三价铁离子用KSCN溶液;
(4)从环保和原料的利用率角度解答;
(5)铜与浓硫酸反应体现了浓硫酸的强氧化性和酸性,铜和氧气和酸反应生成铜离子;
解答:解:(1)因铝与碱反应生成偏铝酸钠和氢气,所以化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
则离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)某气体其固态可用于人工降雨,该气体应该为二氧化碳,二氧化碳的固态为干冰,干冰变成气体时须从外界吸收热量,致水蒸气冷凝,能实现人工降雨,AlCl3溶液中通入二氧化碳,碳酸的酸性比氢氧化铝强,所以能反应,且通过量的二氧化碳生成碳酸氢根离子,
故答案为:CO2;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;途径②;途径①会引入盐酸,氯化钠杂质;
(3)滤液E的成分中的硫酸亚铁中的二价铁离子易被空气中的氧气氧化成三价铁离子,检验三价铁离子的方法是用KSCN溶液,Fe3++3SCN-?Fe(SCN)3血红色,说明E中含有Fe3+,
故答案为:Fe3+;取滤液E少量于试管中,滴入2~3滴 KSCN溶液,若出现血红色,则证明滤液E中含有Fe3+;
(4)途径③的反应:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
途径④的反应:2Cu+O2+2H2SO4(稀)
2CuSO4+2H2O从反应方程式看出产生等量胆矾途径④消耗硫酸少,途径④不会产生污染大气的气体,
故答案为:产生等量胆矾途径④消耗硫酸少;途径④不会产生污染大气的气体;
(5)途径③的反应:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,从反应方程式看出,硫酸中硫从+6价变为产物中的+4价硫,体现强氧化性,金属和酸反应,生成盐,体现了硫酸的酸性,途径④的反应:2Cu+O2+2H2SO4(稀)
2CuSO4+2H2O改成离子反应为2Cu+O2+4H+=2Cu2++2H2O,
故答案为:强氧化、酸;过滤; 2Cu+O2+4H+=2Cu2++2H2O;
则离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)某气体其固态可用于人工降雨,该气体应该为二氧化碳,二氧化碳的固态为干冰,干冰变成气体时须从外界吸收热量,致水蒸气冷凝,能实现人工降雨,AlCl3溶液中通入二氧化碳,碳酸的酸性比氢氧化铝强,所以能反应,且通过量的二氧化碳生成碳酸氢根离子,
故答案为:CO2;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;途径②;途径①会引入盐酸,氯化钠杂质;
(3)滤液E的成分中的硫酸亚铁中的二价铁离子易被空气中的氧气氧化成三价铁离子,检验三价铁离子的方法是用KSCN溶液,Fe3++3SCN-?Fe(SCN)3血红色,说明E中含有Fe3+,
故答案为:Fe3+;取滤液E少量于试管中,滴入2~3滴 KSCN溶液,若出现血红色,则证明滤液E中含有Fe3+;
(4)途径③的反应:Cu+2H2SO4(浓)
| ||
途径④的反应:2Cu+O2+2H2SO4(稀)
| ||
故答案为:产生等量胆矾途径④消耗硫酸少;途径④不会产生污染大气的气体;
(5)途径③的反应:Cu+2H2SO4(浓)
| ||
| ||
故答案为:强氧化、酸;过滤; 2Cu+O2+4H+=2Cu2++2H2O;
点评:本题主要考查了怎样从工业废料中制取纯净物,注意从框图转化中找出有用信息,利用有关的化学反应进行解答,难度中等.

练习册系列答案
相关题目