题目内容
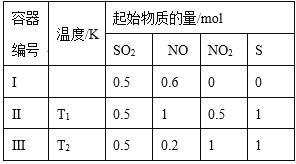
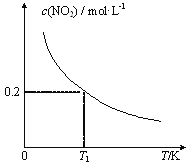
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀。则原溶液中钾离子浓度为( )
A.![]() mol·L-1B.
mol·L-1B.![]() mol·L-1
mol·L-1
C.![]() mol·L-1D.
mol·L-1D.![]() mol·L-1
mol·L-1
【答案】D
【解析】
混合溶液分成两等份,每份溶液浓度相同。一份加入含bmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为BaSO4,根据钡离子与硫酸根守恒可知该份中n(SO42-)=n(BaSO4)=n(BaCl2);一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁,由电荷守恒可知:n(OH-)=2n(Mg2+),再利用电荷守恒可知2n(Mg2+)+n(K+)=2n(SO42-),以此计算。
一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡,则n(SO42-)=bmol;
一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁,则n(Mg2+)=![]() amol,
amol,
由电荷守恒可知2n(Mg2+)+n(K+)=2n(SO42-),
则n(K+)=(2ba)mol,
混合溶液分成两等份,
原混合溶液中钾离子的浓度为![]() mol/L,
mol/L,
故选D。

练习册系列答案
相关题目
【题目】已知X、Y是主族元素,I为电离能,单位是![]() 根据如表所列数据判断,错误的是
根据如表所列数据判断,错误的是
元素 |
|
|
|
|
X | 496 | 4562 | 6912 | 9543 |
Y | 578 | 1817 | 2745 | 11575 |
A. 元素X的常见化合价是![]() 价
价
B. 元素Y是ⅢA族元素
C. X单质的熔点高于Y单质的熔点
D. 若元素X处于第3周期,它的单质可与冷水剧烈反应