题目内容
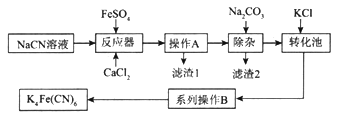
【题目】叠氮化钠(NaN3)是汽车安全气囊最理想的气体发生剂原料。下面是工业水合肼法制备叠氮化钠的工艺流程;

已知NaN3能与AgNO3反应生成白色难溶于水的AgN3;有关物质的物理性质如下表:
熔点℃ | 沸点℃ | 溶解性 | ||
CH3OH | —9 | 64.7 | 与水互溶 | |
水合肼(N2H4H2O) | 2 | 113.5 | 与水、醇互溶, 不溶于乙醚和氯仿 | |
亚硝酸甲酯(CH3ONO) | —17 | —12 | 溶于乙醇、乙醚 |
请回答:
(1)步骤Ⅰ中NaNO2与稀硫酸发生副反应生成两种气体(其中一种气体在空气中可以转化为另一种气体)的离子方程式为___________;步骤Ⅱ中生成NaN3的化学方程式为_______。
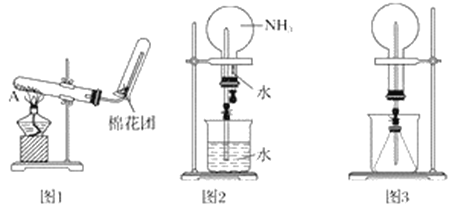
(2)实验室模拟步骤Ⅱ实验装置如下图(装置中冷却水省略,下同):

①仪器a的名称__________________,作用是________________________________。
②根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此可以采取的措施是______________________________。
③图中X处连接的最合适装置应为下图中的_________。
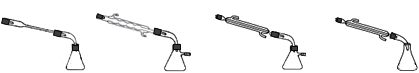
A B C D
(3)步骤Ⅱ、Ⅲ中制备叠氮化钠并对溶液A进行蒸馏的合理操作顺序是__________。
①打开K1、K2,关闭K3 ②打开K3 ③加热 ④关闭K1、K2
(4)步骤Ⅳ对溶液B加热蒸发至溶液体积的1/3,NaN3结晶析出。
①步骤Ⅴ可以用______________洗涤晶体。
A.水 B.乙醇 C.乙醇水溶液 D.乙醚
②沉淀滴定法测定产品纯度,是以淡黄色K2CrO4溶液作指示剂,将AgNO3标准溶液滴入样品溶液,至少量Ag2CrO4出现,即溶液呈淡红色为终点。AgNO3溶液要装在棕色的酸式滴定管里进行滴定,理由是_____________。下列操作合理的是______。
A.滴定管和移液管管尖不可接触锥形瓶内壁
B.滴定时滴液速度应先快后慢,接近终点时一滴一摇
C.滴定过程中可用蒸馏水将锥形瓶壁上粘附的溶液冲下
D.若未等滴定管液面稳定就读数会导致测定结果偏高
E.若发现滴液过量,可回滴样品溶液,至红色褪去
【答案】2NO2-+2H+==NO↑+NO2↑+H2O N2H4+CH3ONO+NaOH==NaN3+CH3OH+3H2O球形冷凝管冷凝回流,平衡气压冷水浴或缓慢通入气体等C①④②③或①②④③CAgNO3溶液溶液显酸性,且AgNO3易见光分解,浓度下降,使测定不准BCD
【解析】
(1)根据其中一种气体在空气中可以转化为另一种气体,可推测生成的气体有一氧化氮和二氧化氮,而根据得失电子守恒和质量守恒可得离子方程式为:2NO2-+2H+==NO↑+NO2↑+H2O;根据流程图可知,产物中含有乙醇和叠氮化钠,所以方程式为:N2H4+CH3ONO+NaOH==NaN3+CH3OH+3H2O;
(2)①A的名称是球形冷凝管,其目的是冷凝回流,平衡气压;②根据实验发现温度在20℃左右反应的选择性和转化率最高,但是该反应属于放热反应不采取措施温度会逐渐升高,影响选择性和转化率,因此可以通过冷水浴或缓慢通入气体等维持反应体系的温度;③收集馏分应采用执行冷凝管,接受的锥形瓶上方应用一个出气口,保持体系内要强等于大气压;
(3)根据亚硝酸甲酯(CH3ONO)的溶沸点很低,所以在通入亚硝酸甲酯时应打开K1、K2,关闭K3,充分反应后,需对混合溶液进行蒸馏提纯,即关闭K1、K2,打开K3,加热进行蒸馏;
(4)①根据反应可知,NaN3结晶中可能含有未反应的水合肼(与水、醇互溶,不溶于乙醚和氯仿)和氢氧化钠,产物CH3OH,可采用乙醇水溶液去除杂质;②AgNO3中的银离子易水解,因此用酸式滴定管,且AgNO3易见光分解,所以酸式滴定管应为棕色,减少AgNO3分解;A.滴定管在滴半滴时需要使溶液悬而不滴,让其沿容器壁流入容器,再用少量水冲洗内壁,故A错误;B.滴定时滴液速度应先快后慢,接近终点时一滴一滴加入并不停摇动,故B正确;C.滴定管在滴半滴时需要使溶液悬而不滴,让其沿容器壁流入容器,再用少量水冲洗内壁,故C正确;D.若未等滴定管液面稳定,滴定关内可能含有气泡,就读数会导致测定结果偏高,故D正确;E.若发现滴液过量,应重新滴定,故E错误;故选BCD。

【题目】KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
![]()
(1)为尽量少引入杂质,试剂①应选用___(填标号)。
A.HCl溶液 | B.H2SO4溶液 | C.氨水 | D.NaOH溶液 |
(2)易拉罐溶解过程中主要反应的化学方程式为________。
(3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是__________。
(4)已知:Kw=1.0×10-14,Al(OH)3![]() AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。