题目内容
11.一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为2Fe2++BH4-+4OH-=2Fe+2H2↑+B(OH)4-.分析 向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,反应中只有Fe、H元素化合价发生变化,结合质量守恒、电荷守恒可写出离子方程式.
解答 解:向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,反应中只有Fe、H元素化合价发生变化,发生氧化还原反应,离子方程式为2Fe2++BH4-+4OH-=2Fe+2H2↑+B(OH)4-,
故答案为:2Fe2++BH4-+4OH-=2Fe+2H2↑+B(OH)4-.
点评 本题考查物质的性质以及离子方程式的书写,题目有利于培养学生的良好的科学素养,侧重于考查学生的分析能力,注意把握提给信息以及物质的性质,为解答该题的关键,难度中等.

练习册系列答案
 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案
相关题目
19.以下化学用语中,正确的是( )
| A. | 乙酸的分子式:C2H4O | B. | 苯的结构简式: | ||
| C. | H2O2的电子式: | D. | 乙醛分子的结构简式:CH3COH |
6.A(g)+3B(g)?2C (g)△H=-b kJ•mol-1,一定条件下,在2L的恒容密闭容器中,反应30min,测得C的物质的量增加了6mol.下列说法正确的是( )
| A. | 第30min时,A的反应速率为0.05 mol•L-1•min-1 | |
| B. | 30min内,C的平均反应速率为0.02 mol•L-1•min-1 | |
| C. | 30min内,V(B)=$\frac{1}{3}$V(A) | |
| D. | 30min内,该反应放出的热量为3b kJ |
20.下列仪器名称为“蒸馏烧瓶”的是( )
| A. |  | B. |  | C. | 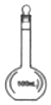 | D. |  |
9.已知反应:①2A-+C2═2C-+A2 ②2C-+B2═2B-+C2 ③2D-+C2═2C-+D2下列说法正确的是( )
| A. | 氧化性:A2>B2>C2>D2 | B. | D-不能被B2氧化 | ||
| C. | 氧化能力:B2>C2>D2 | D. | 还原性:A->B- |
 对N2(g)+3H2(g)?2NH3(g)△H<0反应,其他条件不变情况下,改变起始氢气物质的量(用n(H2)表示),实验结果如下图1表示(图中T表示温度,n表示物质的量);
对N2(g)+3H2(g)?2NH3(g)△H<0反应,其他条件不变情况下,改变起始氢气物质的量(用n(H2)表示),实验结果如下图1表示(图中T表示温度,n表示物质的量); 一定条件下,在水溶液中1mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示.
一定条件下,在水溶液中1mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示.