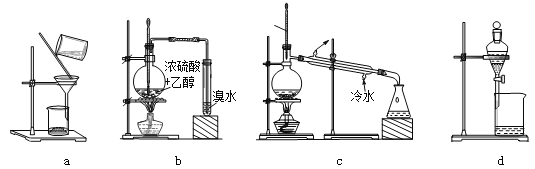
题目内容
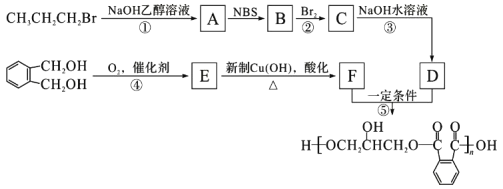
【题目】丙烯是石油化工的重要原料,一定条件下可发生下列转化:
已知:![]()
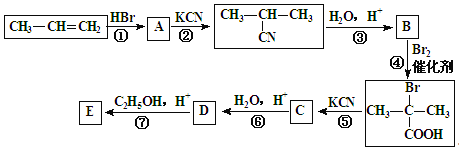
(1)A的结构简式为:______________________;
(2)反应④的类型为:______________________反应;
(3) D与足量乙醇反应生成E的化学方程式为:______________________________________。
(4)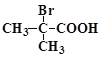 与足量NaOH溶液反应的化学方程式为___________________________。
与足量NaOH溶液反应的化学方程式为___________________________。
(5)B的同分异构体有多种.写出其中既能发生银镜反应,又能发生酯化反应的2种同分异构体的结构简式:___________________________、_______________________________。
【答案】CH3CHBrCH3 取代反应 
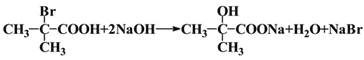 HOCH2CH2CH2CHO CH3CH(OH)CH2CHO或CH3CH2CH(OH)CHO、(CH3)2C(OH)CHO、HOCH2CH(CH3)CHO
HOCH2CH2CH2CHO CH3CH(OH)CH2CHO或CH3CH2CH(OH)CHO、(CH3)2C(OH)CHO、HOCH2CH(CH3)CHO
【解析】
丙烯与HBr发生加成反应生成A,A为溴代烷,A与KCN发生取代反应,生成![]() ,故A为
,故A为![]() ,由信息RCN
,由信息RCN![]() RCOOH,可知B为
RCOOH,可知B为![]() ,
,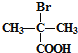 与KCN发生取代反应生成C,C为
与KCN发生取代反应生成C,C为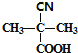 ,C
,C![]() D,由信息RCN
D,由信息RCN![]() RCOOH可知D为
RCOOH可知D为 ,
, 与足量的乙醇发生酯化反应生成E,E为
与足量的乙醇发生酯化反应生成E,E为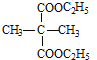 ;
;
(1)由上述分析可知,A的结构简式为 ![]() ;
;
(2)反应④是![]() 与溴反应生成
与溴反应生成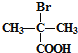 ,属于取代反应;
,属于取代反应;
(3) 与足量的乙醇发生酯化反应生成
与足量的乙醇发生酯化反应生成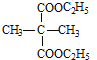 ,反应化学方程式为
,反应化学方程式为 ;
;
(4)![]() 与足量NaOH溶液反应,发生卤代烃的水解溶液与羧酸的中和反应,反应方程式为:
与足量NaOH溶液反应,发生卤代烃的水解溶液与羧酸的中和反应,反应方程式为: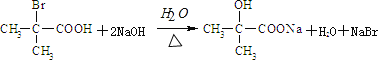 ;
;
(5)![]() 的同分异构体有多种,其中既能发生银镜反应,又能发生酯化反应,说明分子中含有醛基-CHO与羟基-OH,符合结构的有机物为:
的同分异构体有多种,其中既能发生银镜反应,又能发生酯化反应,说明分子中含有醛基-CHO与羟基-OH,符合结构的有机物为:、
![]() 等。
等。

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目