题目内容
铅蓄电池的两极分别是Pb、PbO2,电解质溶液为30%硫酸,工作时反应为:
Pb+PbO2+2H2SO4 2PbSO4+2H2O 下列结论正确的是(B )
2PbSO4+2H2O 下列结论正确的是(B )
Pb+PbO2+2H2SO4
 2PbSO4+2H2O 下列结论正确的是(B )
2PbSO4+2H2O 下列结论正确的是(B )| A.PbO2为正极,被氧化 | B.电池电解质溶液的密度不断减小 |
| C.c(H+)逐渐增大 | D.H+向负极移动 |
B
在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。放电相当于原电池,所以二氧化铅是正极,被还原,A不正确。放电时生成硫酸铅沉淀,所以密度减小,B正确。放电消耗氢离子,浓度降低,C不正确。阳离子向正极移动,D不正确。答案选B。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
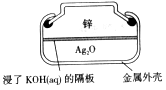
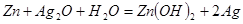
 作负极
作负极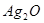 极
极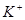 向
向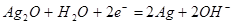
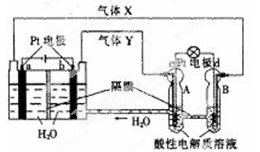
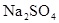 试液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:( )
试液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:( )
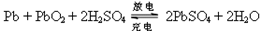 ,下列说法正确的是
,下列说法正确的是