题目内容
【题目】室温下,用相同浓度的NaOH溶液分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是
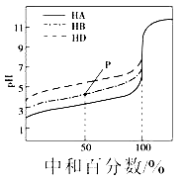
A.三种酸的电离常数关系: KHA>KHB>KHD
B.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
C. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
D.当中和百分数达100%时,将三种溶液混合后:
c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
【答案】B
【解析】A项,相同浓度的三种酸(HA、HB和HD)溶液,pH越小,酸性越强,三种酸的电离常数关系: KHA>KHB>KHD,正确;B项,pH=7时,各溶液中钠离子浓度等于酸根离子浓度,三种溶液中加的NaOH溶液不一样,酸根离子浓度不一样,错误;C项,滴定至P点时,溶液中NaB和HB浓度相同,溶液显酸性,c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-),正确;D项,当中和百分数达100%时,将三种溶液混合后,根据质子守恒,c(HA)+c(HB)+c(HD)=c(OH-)-c(H+),正确。

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
【题目】下列分离或提纯有机物的方法正确的是( )
选项 | 待提纯物质 | 杂质 | 除杂试剂及主要操作方法 |
A | 乙烷 | 乙烯 | 酸性 KMnO4溶液, 洗气 |
B | 溴苯 | 溴 | NaOH 溶液,分液 |
C | 乙酸 | 乙醇 | 金属钠,蒸馏 |
D | 乙醇 | 水 | 生石灰,过滤 |
A. A B. B C. C D. D