题目内容
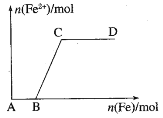
【题目】在一定量的稀HNO3中慢慢加入铁粉,得到的Fe2+的物质的量(纵坐标)与所加的铁粉的物质的量(横坐标)的关系如图所示,AB段与BC段所需Fe的质量比为( )
A.2:1B.1:2C.1:4D.3:8
【答案】A
【解析】
在一定量的稀HNO3中缓慢加入铁粉,开始时反应Fe+4HNO3═Fe(NO3)3+NO↑+2H2O此时铁元素在溶液中以Fe3+存在,在B点时,硝酸恰好反应完全;继续加铁粉,发生Fe+2Fe3+═3Fe2+,此时溶液中Fe2+的量逐渐增多,Fe3+的量逐渐减少,即BC段;在C点时,溶液中的Fe3+恰好完全反应,此时继续加入的铁粉不再反应,溶液中的Fe2+的量不再增多,即CD段。设AB段消耗amol Fe,生成amol Fe3+,根据反应Fe+2Fe3+═3Fe2+可知BC段需要消耗![]() amol Fe,则AB段与BC段所需Fe的质量比为2:1,故选A。
amol Fe,则AB段与BC段所需Fe的质量比为2:1,故选A。

练习册系列答案
相关题目