��Ŀ����
��Ⱦ�뻷�������Ѿ���Ϊ�����ҹ������ŵ�һ�����⣬��Ⱦ��Ϊ������Ⱦ��ˮ��Ⱦ��������Ⱦ�ȡ�
��1��Ϊ�˼��ٿ�����SO2���ŷţ�����ȡ�Ĵ�ʩ�У�
�ٽ�úת��Ϊ�������ȼ�ϡ�
��֪��H2(g)��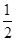 O2(g)=H2O(g) ��H1����241.8 kJ��mol��1
O2(g)=H2O(g) ��H1����241.8 kJ��mol��1
C(s)��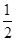 O2(g)=CO(g) ��H2����110.5 kJ��mol��1
O2(g)=CO(g) ��H2����110.5 kJ��mol��1
д����̿��ˮ������Ӧ���Ȼ�ѧ����ʽ�� ��
�÷�Ӧ��ƽ�ⳣ������ʽΪK�� ��
��ϴ�Ӻ�SO2���������������ʿ���ϴ�Ӽ����� ��ѡ����ţ���
a��Ca(OH)2 b��CaCl2 c��Na2CO3 d��NaHSO3
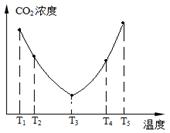
��2��Ϊ�˼��ٿ����е�CO2��Ŀǰ��̼�����ڽ������������ŷ��о�����Ҫ�����ã���̼������(NH4)2CO3����ӦΪ��(NH4)2CO3(aq)��H2O(l)��CO2(g)��2NH4HCO3(aq) ��H3Ϊ�о��¶ȶ�(NH4)2CO3����CO2Ч�ʵ�Ӱ�죬��ij�¶�T1�£���һ������(NH4)2CO3��Һ�����ܱ������У�������һ������CO2���壨�õ�����Ϊϡ�ͼ�������tʱ�̣����������CO2�����Ũ�ȡ�Ȼ��ֱ����¶�ΪT2��T3��T4��T5�£�����������ʼʵ���������䣬�ظ�����ʵ�飬������ͬʱ����CO2����Ũ�ȣ����ϵ��ͼ����
�٦�H3 0(�����������������)��
����T4��T5����¶����䣬������CO2����Ũ�ȱ仯���Ƶ�ԭ���ǣ� ��
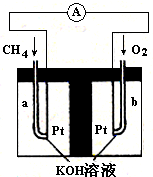
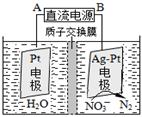
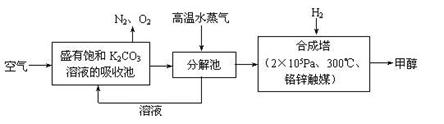
��3�������������͵绯ѧ���ⷨ����������ˮ�������ε���Ⱦ��
�ٴ����������У���H2��NO3-��ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ����Ӧ���ӷ���ʽΪ�� ��
�ڵ绯ѧ����NO3-��ԭ����ͼ����Դ����Ϊ�� ��ѡ���A����B������������ӦʽΪ�� ��
��1��Ϊ�˼��ٿ�����SO2���ŷţ�����ȡ�Ĵ�ʩ�У�
�ٽ�úת��Ϊ�������ȼ�ϡ�
��֪��H2(g)��
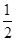 O2(g)=H2O(g) ��H1����241.8 kJ��mol��1
O2(g)=H2O(g) ��H1����241.8 kJ��mol��1C(s)��
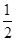 O2(g)=CO(g) ��H2����110.5 kJ��mol��1
O2(g)=CO(g) ��H2����110.5 kJ��mol��1д����̿��ˮ������Ӧ���Ȼ�ѧ����ʽ�� ��
�÷�Ӧ��ƽ�ⳣ������ʽΪK�� ��
��ϴ�Ӻ�SO2���������������ʿ���ϴ�Ӽ����� ��ѡ����ţ���
a��Ca(OH)2 b��CaCl2 c��Na2CO3 d��NaHSO3
��2��Ϊ�˼��ٿ����е�CO2��Ŀǰ��̼�����ڽ������������ŷ��о�����Ҫ�����ã���̼������(NH4)2CO3����ӦΪ��(NH4)2CO3(aq)��H2O(l)��CO2(g)��2NH4HCO3(aq) ��H3Ϊ�о��¶ȶ�(NH4)2CO3����CO2Ч�ʵ�Ӱ�죬��ij�¶�T1�£���һ������(NH4)2CO3��Һ�����ܱ������У�������һ������CO2���壨�õ�����Ϊϡ�ͼ�������tʱ�̣����������CO2�����Ũ�ȡ�Ȼ��ֱ����¶�ΪT2��T3��T4��T5�£�����������ʼʵ���������䣬�ظ�����ʵ�飬������ͬʱ����CO2����Ũ�ȣ����ϵ��ͼ����

�٦�H3 0(�����������������)��
����T4��T5����¶����䣬������CO2����Ũ�ȱ仯���Ƶ�ԭ���ǣ� ��
��3�������������͵绯ѧ���ⷨ����������ˮ�������ε���Ⱦ��
�ٴ����������У���H2��NO3-��ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ����Ӧ���ӷ���ʽΪ�� ��
�ڵ绯ѧ����NO3-��ԭ����ͼ����Դ����Ϊ�� ��ѡ���A����B������������ӦʽΪ�� ��

��1���� C(s)��H2O(g) �� CO(g) ��H2(g) ��H����131.3kJ��mol��1 k��c CO)��c( H2)/c(H2O)
�� a c����1�֣�
��2���� <
�� T4��T5 ��Ӧ��ƽ�⣬����ӦΪ���ȷ�Ӧ�������¶ȵ����ߣ�ƽ�������ƶ���CO2������Ч�ʽ��ͣ���NH4HCO3���ַֽ⣬��˼��������֣���
��3����2 NO3����5H2 N2��2OH����4H2O
N2��2OH����4H2O
��A 2 NO3����12 H+��10e��= N2����6H2O
�� a c����1�֣�
��2���� <
�� T4��T5 ��Ӧ��ƽ�⣬����ӦΪ���ȷ�Ӧ�������¶ȵ����ߣ�ƽ�������ƶ���CO2������Ч�ʽ��ͣ���NH4HCO3���ַֽ⣬��˼��������֣���
��3����2 NO3����5H2
 N2��2OH����4H2O
N2��2OH����4H2O��A 2 NO3����12 H+��10e��= N2����6H2O
�����������1���������������Ȼ�ѧ����ʽ��ʽ����ʽ����C(s)��H2O(g) �� CO(g) ��H2(g) ��H����131.3kJ��mol��1�����Լ�Ca(OH)2��Na2CO3���������Ӧ��������Ϊ�����ռ�����2���ٸ�ͼ����ͬʱ��ʱ�ⶨ�Ķ�����̼��Ũ�ȣ��¶�Խ�߷�Ӧ����Խ�죬�ȴ�ƽ�⣬����ͼ���T3Ϊ�磬������ƽ�����ߣ��ݴ˷����¶ȸ߶�����̼������ƽ�������ƶ�������ӦΪ���ȷ�Ӧ����H3< 0����T4��T5 ��Ӧ��ƽ�⣬����ӦΪ���ȷ�Ӧ�������¶ȵ����ߣ�ƽ�������ƶ���CO2������Ч�ʽ��ͣ���3���÷�Ӧ�������ϼ����ߣ�������Һ������ǿ����������OH�����ɴ���д����ʽ��������B�����ĵ缫NO3���õ���������N2��Ϊ��������AΪ������BΪ������

��ϰ��ϵ�д�
 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д� ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
�����Ŀ
 2B(g)��ǰ110 s�ڵķ�Ӧ���̡�
2B(g)��ǰ110 s�ڵķ�Ӧ���̡�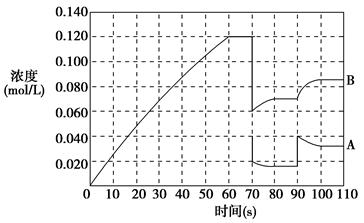

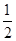 O2(g ) = CO2( g ) ��H����283.0 kJ / mol ��
O2(g ) = CO2( g ) ��H����283.0 kJ / mol �� H++CN������Ħ�HΪ kJ��mol��1
H++CN������Ħ�HΪ kJ��mol��1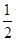 O2(g)��H��242 kJ��mol��1
O2(g)��H��242 kJ��mol��1
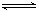 2NH3��g����H��0����ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
2NH3��g����H��0����ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
 2H2O��l�� ��H����483��6 kJ��mol
2H2O��l�� ��H����483��6 kJ��mol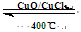 2Cl2(g)+2H2O(g) ��H=" ��115.6" kJ/mol
2Cl2(g)+2H2O(g) ��H=" ��115.6" kJ/mol 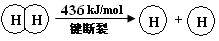
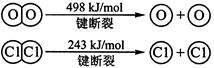
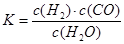 ��������Ӧ�Ļ�ѧ����ʽΪ��
��������Ӧ�Ļ�ѧ����ʽΪ�� 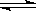 2NH3(g) ��H<0 ��K=0.5����400��ʱ����0.5L�ķ�Ӧ�����н��кϳɰ���Ӧ��һ��ʱ����N2��H2��NH3�����ʵ����ֱ�Ϊ2mol��1mol��2mol�����ʱ��Ӧv(N2)�� v(N2)���������������������ȷ������1�֣�
2NH3(g) ��H<0 ��K=0.5����400��ʱ����0.5L�ķ�Ӧ�����н��кϳɰ���Ӧ��һ��ʱ����N2��H2��NH3�����ʵ����ֱ�Ϊ2mol��1mol��2mol�����ʱ��Ӧv(N2)�� v(N2)���������������������ȷ������1�֣�