题目内容
金属铜不溶于稀硫酸,但可溶于铁盐溶液。现将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化)。
(1)写出铜溶解于上述混合溶液的离子方程式_______________________________________。
(2)若铜完全溶解时,溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶解铜的质量是_________g,溶液中的c(SO42—)=__________mol/L。
(3)若欲在如图所示的装置中发生(1)中的反应,则:X极是 (正、负极),电极反应式 。Y极的材料是 ,电极反应式 。

(1)Cu+2Fe3+=Cu2++2Fe2+(2分)
(2) 0.64(2分) 0.3(2分)
(3)负极,Cu-2e-=Cu2+ 碳(石墨、金、铂、银), 2Fe3++2e-=2Fe2+(各1分)
【解析】
试题分析: (1)铜和铁离子反应生成亚铁离子和铜离子,离子反应方程式为:Cu+2Fe3+═Cu2++2Fe2+,故答案为:Cu+2Fe3+═Cu2++2Fe2+;
(2)若铜完全溶解时,溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则c(H+)=c(Cu2+)=0.1mol/L,根据原子守恒得m(Cu)=CVM=0.1mol/L×0.1L×64g/mol=0.64g,根据电荷守恒得2c(SO42-)=c(H+)+2c(Cu2+)+3c(Fe3+)=6c(H+)=0.6mol/L,c(SO42-)=0.3mol/L,故答案为:0.64,0.3mol/L;
(3)若欲在如图所示的装置中发生(1)中的反应,则铜电极是负极,不如铜活泼的金属或导电的非金属作正极,所以X电极是负极,负极上电极反应式为:Cu-2e-═Cu2+,碳(石墨、金、铂、银)作正极,正极上铁离子得电子发生还原反应,电极反应式为:2Fe3++2e-═2Fe2+,故答案为:负极,Cu-2e-═Cu2+,碳(石墨、金、铂、银),2Fe3++2e-═2Fe2+。
考点:本题考查的是氧化还原反应和原电池的基础知识。

 阅读快车系列答案
阅读快车系列答案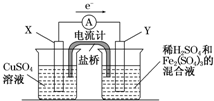 (2010?宝鸡一模)(2011?长春质检)金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化)
(2010?宝鸡一模)(2011?长春质检)金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化) 金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化).
金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化).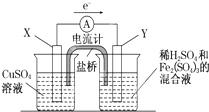 金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化).
金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化).