题目内容
【题目】下列制备FeSO4最适宜的方法是
A.FeO与稀硫酸反应 B.过量的铁与稀硫酸反应
C.FeCO3与稀硫酸反应 D.Fe(OH)2与稀硫酸反应
【答案】B
【解析】
试题分析:B.无论Fe是否过量,Fe和稀硫酸都只生成硫酸亚铁,过量的Fe和稀硫酸反应生成硫酸亚铁和氢气,且稀硫酸没有剩余,所以该方法制备较适宜,故B选;A.FeO和稀硫酸反应生成硫酸亚铁和水,稀硫酸如果过量导致溶液中溶质有两种,故A不选;C.碳酸铁和稀硫酸反应生成硫酸亚铁、二氧化碳和水,如果稀硫酸过量导致溶液中溶质有两种,故C不选;D.氢氧化亚铁很不稳定易氧化为氢氧化铁,和稀硫酸反应会有硫酸铁生成,故D不选;故选B。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的的是( )
混合物 | 试剂 | 分离方法 | |
A | 苯(苯酚) | 溴水 | 过滤 |
B | 乙烷(乙烯) | 氢气 | 加热 |
C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
D | 溴苯(溴) | NaOH溶液 | 分液 |
A. AB. BC. CD. D
【题目】(l)基态As原子的核外电子排布式为[Ar]______,有________个未成对电子。
(2) As与N是同主族元素,从原子结构角度分析:为什么As的最高价含氧酸H3AsO4是三元酸(含三个轻基),而N的最高价含氧酸HNO3是一元酸(只含一个烃基)______。
(3)比较下列氢化物的熔点和沸点,分析其变化规律及原因__________。
(4) Na3AsO3中Na、As、O电负性由大至小的顺序是______。AsO33-的空间构型为___, AsO33-中As的杂化轨道类型为_______杂化。
(5)砷化稼(GaAs)为黑灰色固体,熔点为1238℃。该晶体属于___晶体,微粒之间存在的作用力是_________。
NH3 | PH3 | AsH3 | SbH3 | |
熔点/K | 195.3 | 140.5 | 156.1 | 185 |
沸点/K | 239.6 | 185.6 | 210.5 | 254.6 |
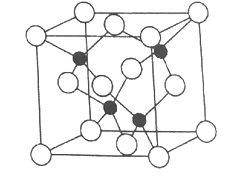
(6)图为GaAs的晶胞,原子半径相对大小是符合事实的,则白球代表____原子。
己知GaAs的密度为5.307g·cm3, Ga和As的相对原子质量分别为69.72、74.92,求晶胞参数a=______pm (列出计算式即可)。