题目内容
【题目】下列溶液,一定呈中性的是
A. 由等体积、等物质的量浓度的硫酸跟NaOH溶液混合后所形成的溶液
B. c(H+)=1.0×10-7mol·L-1的溶液
C. pH=7的溶液
D. c(H+)=![]() 的溶液(Kw为该温度下水的离子积常数)
的溶液(Kw为该温度下水的离子积常数)
【答案】D
【解析】
试题A、由等体积、等物质的量浓度的硫酸跟NaOH溶液混合后所形成的溶液,因为硫酸中氢离子的物质的量大于氢氧化钠中氢氧根离子的物质的量,所以溶液呈酸性,错误;B、常温时c(H+)=1.0×10-7mol·L-1的溶液为中性,但未指明温度时,不能判断溶液的酸碱性,错误;C、常温时pH=7的溶液为中性,但未指明温度时,不能判断溶液的酸碱性,错误;D、因为c(H+) ×c(OH-)=KW,所以c(H+)=![]() 时,说明c(H+) =c(OH-),此溶液一定是中性溶液,正确,答案选D。
时,说明c(H+) =c(OH-),此溶液一定是中性溶液,正确,答案选D。

 阅读快车系列答案
阅读快车系列答案【题目】无机化合物可根据其组成和性质进行分类,如下所示:
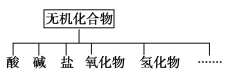
(1)上面所示的物质分类方法名称是________。
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥处。
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①HCl ②______ | ③______ ④Ba(OH)2 | ⑤Na2CO3 ⑥______ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(3)写出实验室由⑩制备O2的化学方程式___________________________________。
【题目】以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)CO(g)+H2(g)△H=+131.3kJmol﹣1
①该反应在常温下_______自发进行(填“能”与“不能”);
②一定温度和压强下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是__________(填字母,下同)
a.容器中的压强不变
b.1mol H﹣H键断裂的同时断裂2mol H﹣O
c.c(CO)=c(H2)
d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)CO2(g)+H2(g),得到如表三组数据:
实验组 | 温度 ℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
① | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
② | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
③ | 900 | a | b | c | d | t |
①该反应为_________(填“吸”或“放”)热反应;实验②条件下平衡常数K=___________。
②实验①中从反应开始至平衡以CO2表示的平均反应速率为V(CO2)=____________(取小数点后两位)
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)CH3H(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJmol﹣1)的变化.在体积为1L 的恒容密闭容器中,充入1mol CO2和3mol H2, 下列措施中能使c (CH3OH)增大的是_____________.

A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来
D.再充入1mol CO2和3mol H2.
【题目】近期我国冀东渤海湾发现储量达10亿吨的大型油田,下列说法正确的是( )
A. 石油属于可再生矿物能源 B. 石油主要含有碳、氢两种元素
C. 石油的裂化是物理变化 D. 石油分馏的各馏分均是纯净物
【题目】利用工业炼铅产生的锌灰(主要成分为ZnO、PbO、FeO、MnO2、CuO)可回收制备ZnCl2,工艺流程如下:

回答下列问题
(1)“浸取”实验中,反应体系的温度、反应时间对锰脱除效果的影响如下表,则适合的温度和反应时间分别是________、________。
表1 温度对锰脱除效果的影响
温度/℃ | ρ(Mn2+)/mg/L | 除锰率/% |
10 | 0.325 | 87.9 |
30 | 0.341 | 89.5 |
50 | 0.424 | 84.3 |
70 | 0.646 | 76.1 |
表2 反应时间对锰脱除效果的影响
时间/h | ρ(Mn2+)/mg/L | 除锰率/% |
1.0 | 0.995 | 63.1 |
1.5 | 0.794 | 70.6 |
2.0 | 0.328 | 87.9 |
2.5 | 0.325 | 87.9 |
(2)“滤渣1”的主要成分是________。
(3)H2O2溶液的作用是___________,已知“滤渣2”的主要成分是Fe(OH)3,则氧化锌的作用是____________。“置换”实验中发生反应的离子方程式有Zn+Pb2+=Pb+Zn2+、_________。
(4)由锌灰制取金属锌可采用碱溶解,然后电解浸取液,已知:ZnO溶于NaOH溶液中生成[Zn(OH)4]2,则阴极的电极反应为____________________________________________。
(5)ZnCl2晶体溶解于饱和Na2CO3溶液中,得到6.46 g的碱式碳酸锌[Znx(CO3)y(OH)z],为了测定其组成,充分加热分解,产生的气体依次通入浓硫酸和碱石灰,质量分别增重了0.72g和0.88g,则该碱式碳酸锌的化学式为________________。