题目内容
【题目】(1)下列物质中,能导电的是 ,属于电解质的是 (填序号)。
①氨气、②氨水、③NH3·H2O、④硫酸溶液、⑤干冰、⑥BaSO4、⑦金刚石
(2)将等物质的量的①Na、②Na2O、③Na2O2、④NaOH投入相同质量的水中,所得溶液浓度由大到小的顺序为 。如果将等物质的量换成等质量则 。(填序号)
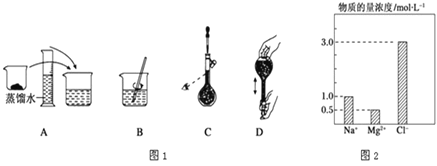
(3)如图表示某同学配制480mL 0.5mol/L 的NaOH溶液的部分操作示意图,其中有错误的是___________,这样操作所配制的溶液比要求的浓度要___________ (填“偏高”、“偏低”、“不影响”)。配制应称取___________gNaOH。
【答案】(14分)(1) ②④ ,③⑥
(2)②Na2O=③Na2O2>①Na>④NaOH ③①Na>②Na2O>③Na2O2>④NaOH
(3)C; 偏低; 10.0
【解析】试题分析:(1)①氨气是非电解质,不导电;②氨水是混合物,能导电,不是电解质,也不是非电解质;③NH3·H2O是电解质,但不导电;④硫酸溶液是混合物,能导电,不是电解质,也不是非电解质;⑤干冰是非电解质,不导电;⑥BaSO4是难溶于水的盐,熔融时导电,是电解质,晶体本身不导电;⑦金刚石是单质,不导电,不是电解质,也不是非电解质;
(2)等物质的量的①Na②Na2O③Na2O2④NaOH,根据Na原子守恒得,n(NaOH)大小顺序是②=③>①=④,Na与水反应消耗水,而氢氧化钠不消耗水,根据c=n/V知,溶液物质的量浓度大小顺序是②=③>①>④;
一般情况下,等质量的①Na②Na2O③Na2O2④NaOH,Na质量分数关系为①>②>③>④,Na的质量分数越大,Na的质量越大,投入相同质量的水中,所得溶液浓度越大,因此溶液物质的量浓度大小顺序是①>②>③>④;
(3)(1)定容时眼睛与刻度线相平,不能俯视或仰视;定容时,眼睛仰视刻度线,溶液的液面超过刻度线,溶液的体积偏大,浓度偏小;实际配制溶液体积为500mL,则所需NaOH的质量为0.5mol/L×0.5L×40g/mol=10.0g。