题目内容
【题目】如图带漏斗U型管中装有足量的煤油和水的混合物,静置后投入一小块碱金属.可观察到金属在煤油和水的界面a附近上下往复运动,下列说法不正确的是( )
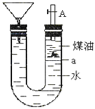
A. 此碱金属可能是钾或钠
B. 反应一段时间煤油会燃烧
C. 碱金属上下运动是由于与水反应产生了氢气
D. 若是金属锂则不能观察到上述现象
【答案】B
【解析】试题分析:Na、K的密度小于水但大于煤油,Na、K和水反应生成碱和氢气,反应中金属处在没有氧气的环境中,不能燃烧,据此分析解答.
解:A.Na、K的密度小于水但大于煤油,Na、K和水反应生成碱和氢气,金属在煤油和水的界面a附近上下往复运动,则该金属可能是钠或K,故A正确;
B.反应中金属处在没有氧气的环境中,不能燃烧,故B错误;
C.碱金属上下运动是由于与水反应产生了氢气,使金属受力不均导致的,故C正确;
D.金属锂的密度小于煤油,所以会浮在煤油表面,所以若是金属锂则不能观察到上述现象,故D正确;
故选B.

【题目】I:已知:反应aA(g)+bB(g) ![]() cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
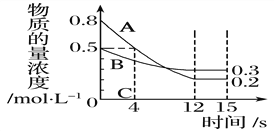
(1)经测定前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为_______________________
(2)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1; 乙:v(B)=0.12 mol·L-1·s-1; 丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为__________________(用甲、乙、丙表示)。
Ⅱ: 某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
氢气体积/mL | 50 | 120 | 224 | 392 | 472 | 502 |
(3)哪一时间段反应速率最大__(填0~1、1~2、2~3、3~4、4~5、5~6 min,下同),原因是_______________________________________________________
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是__________(填字母)
A.CH3COONa B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
Ⅲ:(5)下列说法可以证明H2(g)+I2(g)![]() 2HI(g)已达平衡状态的是______________________
2HI(g)已达平衡状态的是______________________
A.单位时间内生成n mol H2的同时,生成n mol HI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=![]() v(HI)
v(HI)
E.温度和体积一定时,容器内压强不再变化
F.温度和体积一定时,混合气体的密度不再变化