题目内容
【题目】下列图示与对应的叙述相符的是( )
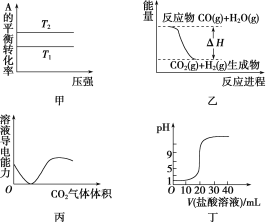
A.由图甲可以判断:对于反应A(g)+B(g) ![]() 2C(g),若T1>T2,则ΔH<0
2C(g),若T1>T2,则ΔH<0
B.图乙表示可逆反应CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH>0
CO2(g)+H2(g) ΔH>0
C.图丙表示CO2通入饱和Na2CO3溶液中,溶液导电性变化
D.图丁表示0.1 mol·L-1的盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液pH随加入盐酸体积的变化
【答案】A
【解析】选A。A项,升高温度,A的平衡转化率减小,平衡左移,则ΔH<0;B项,ΔH应小于0;C项,生成NaHCO3晶体,溶液中离子带电荷总数减小,导电能力减弱,但不为0,之后生成H2CO3,导电能力变化不大;D项,曲线中的pH应从大到小。

【题目】七水硫酸镁(MgSO4·7H2O)可用于印染加重剂,制造瓷器、颜料和防火材料。在医药上用作泻剂,在徽生物工业作培养基成分等。可利用化工厂生产硼砂的废渣——硼镁泥制取七水硫酸镁(MgSO4·7H2O),硼镁泥的主要成分是MgCO3,还含有其它杂质(MgO、Na2B4O7、SiO2、Fe2O3、CaO、Al2O3、MnO等)。
硼镁泥制取七水硫酸镁的工艺流程图如下:

表l:部分阳离子开好成淀和完全沉淀时溶液的pH
Fe3+ | Fe2+ | Mn2+ | Mg2+ | Al3+ | |
开始沉淀的pH | 1.9 | 7.9 | 8.6 | 9.6 | 3.1 |
完全沉淀的pH | 3.2 | 9.0 | 10.l | 11 | 5.4 |
据此试回答下列问题:
(1)写出生成H3BO3的离子方程式______________。
(2)NaClO具有强氧化性,能直接将溶液中Fe2+和Mn2+分别氧化成______(填化学式)。
(3)能否直接控制pH除去Mn2+______,理由__________。
(4)若检验时溶液呈红色,说明滤液B中还含有_______未除尽(填离子符号),应补加_______再煮沸趁热过滤(填化学式)。
(5)沉淀D的化学式_______________。