题目内容
【题目】某课外小组研究铝土矿中Al2O3的含量。已知铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
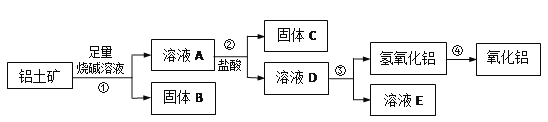
(1)固体B的主要用途有(写出1条即可)_______。
(2)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是_____;_____;第③步中,生成氢氧化铝的离子方程式是______。
(3)将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是______(保留一位小数)
(4)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5 mol 碳单质,转移1mol电子,反应的化学方程式是______。
【答案】【答题空1】炼铁原料、用作涂料、油漆等【答题空2】Al2O3+2OH-=2AlO2-+H2O【答题空3】SiO2+2OH-=SiO32-+H2O【答题空4】Al3++3NH3·H2O=Al(OH)3↓+3NH4+【答题空5】65.4%【答题空6】Al2O3+3Cl2+3C![]() 2AlCl3+3CO
2AlCl3+3CO
【解析】
【试题分析】
由题意,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等,所以加入足量烧碱溶液Fe2O3不反应,Al2O3和SiO2与烧碱溶液反应生成NaAlO2和Na2SiO3,向所得溶液中加入盐酸生成NaCl、AlCl3和H2SiO3(或SiO2),再向所得溶液中加入过量氨水,生成NaCl、NH4Cl、Al(OH)3,加热Al(OH)3分解生成Al2O3。
(1)因为Fe2O3不与氢氧化钠溶液反应,所以固体B为Fe2O3,Fe2O3可用做炼铁原料,Fe2O3俗称铁红,可用作涂料、油漆等。
(2)铝土矿的主要成分Al2O3和少量SiO2与烧碱反应生成NaAlO2和Na2SiO3,离子方程式为:Al2O3+2OH-=2AlO2-+H2O、SiO2+2OH-=SiO32-+H2O ;流程第③步中Al3+与NH3H2O生成Al(OH)3和NH4+,离子方程式为:Al3++3NH3·H2O=Al(OH)3↓+3NH4+。
(3)Al(OH)3受热分解生成Al2O3,转化关系为2 Al(OH)3~ Al2O3,由题意所得氢氧化铝固体的质量与原铝土矿质量相等,所以该铝土矿中Al2O3的质量分数是:![]()
(4)由题意,用Al2O3与C、Cl2在高温条件下反应制取AlCl3,每消耗0.5 mol 碳单质,转移1mol电子,所以C的化合价由0→+2价,生成CO,反应化学方程式为:Al2O3+3Cl2+3C ![]() 2AlCl3+3CO
2AlCl3+3CO
