题目内容
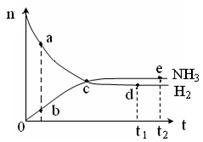
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
 2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
| A.点a的n(H2)和点b的n(NH3)比值为3:2 |
| B.点 c处反应达到平衡 |
| C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样 |
| D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大 |
D
根据图像可知,选项A不正确。C点氢气和氨气的物质的量还是变化的,所以反应没有达到平衡状态,B不正确。点d (t1时刻) 和点 e (t2时刻) 都是在相同条件下的平衡状态,氮气的物质的量相同,C不正确。反应是放热反应,所以升高温度,平衡向逆反应方向移动,氢气的物质的量增大,D正确,答案选D。

练习册系列答案
相关题目
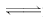 CH3OH(g).
CH3OH(g).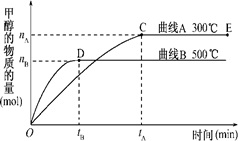
 ?zC(g),平衡时测得A的浓度为1.0 mol/L,保持温度不变,将容器的容积扩大到原来的2倍,达到新平衡后,测得A的浓度降低为0.60 mol/L。下列有关判断正确的是( )
?zC(g),平衡时测得A的浓度为1.0 mol/L,保持温度不变,将容器的容积扩大到原来的2倍,达到新平衡后,测得A的浓度降低为0.60 mol/L。下列有关判断正确的是( ) xC(g)达到平衡后,C的体积分数为W%。若维持容积和温度不变,按1.4 molA、0.7molB、1.2molC为起始物质,达到平衡后C的体积分数仍为W%,则x的值为:
xC(g)达到平衡后,C的体积分数为W%。若维持容积和温度不变,按1.4 molA、0.7molB、1.2molC为起始物质,达到平衡后C的体积分数仍为W%,则x的值为: 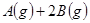

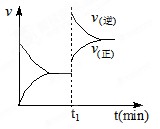
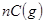 (正反应放热)生成物C的浓度随压强变化并建立平衡的关系图,则
(正反应放热)生成物C的浓度随压强变化并建立平衡的关系图,则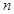 值与压强
值与压强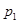 、
、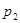 的关系正确的是
的关系正确的是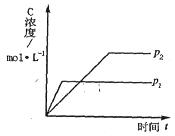
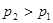 ,
,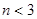
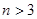
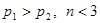
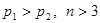
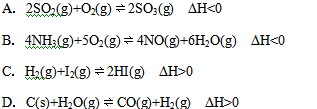
 2NH3(g),
2NH3(g),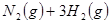

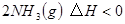 ,工业上选择的适宜条件为:
,工业上选择的适宜条件为: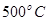 、铁作催化剂、
、铁作催化剂、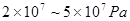 。下列说法正确的是
。下列说法正确的是