题目内容
(6分)把0.04 mol X气体和0.06 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:4X(g)+5Y(g)===nZ(g)+6W(g);2 min末生成0.03 mol W。若测知以Z的浓度变化表示的反应速率为0.005 mol·(L·min)-1。试计算:
(1)前2 min内用X的浓度变化表示的平均反应速率为 ;
(2)化学方程式中n的值是 。
(1)前2 min内用X的浓度变化表示的平均反应速率为 ;
(2)化学方程式中n的值是 。
0.005 mol/(L·min); 4
试题分析:(1)因为在2 min末生成0.03 mol W,则根据方程式中X与M的物质的量的比为4:6,所以消耗的X的物质的量为0.02mol。因此前2 min内用X的浓度变化表示的平均反应速率为(0.02mol÷2 L)÷2min=0.005 mol/(L·min)。(2)V(Z)=0.005 mol·(L·min)-1,所以在前2分钟内Z的物质的量变化:0.005 mol·(L·min)-1×2min×2L=0.02mol.因为在化学方程式中,物质的方程式前边的系数比等于其物质的量的比,所以n:6="0.02mol:" 0.03 mol。解得n=4。

练习册系列答案
相关题目
 H=-1266.8kJ·mol-1
H=-1266.8kJ·mol-1
 Si3N4 + 6CO,该反应过程中的能量变化如图⑵所示;回答下列问题:
Si3N4 + 6CO,该反应过程中的能量变化如图⑵所示;回答下列问题: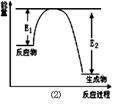

 (正)
(正) 
 Pb(s) + CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表
Pb(s) + CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表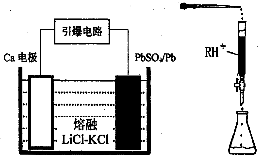
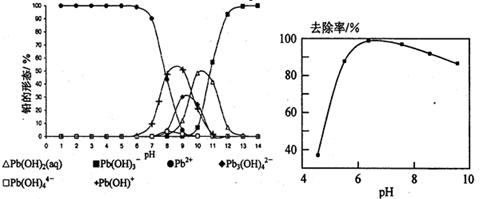
 H2(g)+I2(g)。若HI浓度由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么HI浓度由0.07 mol·L-1降到0.05 mol·L-1时所需反应的时间为
H2(g)+I2(g)。若HI浓度由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么HI浓度由0.07 mol·L-1降到0.05 mol·L-1时所需反应的时间为
 2AB3(g)的ΔH>0
2AB3(g)的ΔH>0
 2SO3(g) △H=-190 kJ·mo1-1
2SO3(g) △H=-190 kJ·mo1-1