题目内容
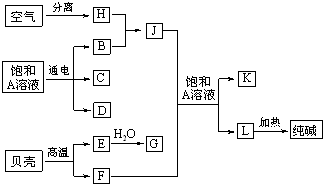
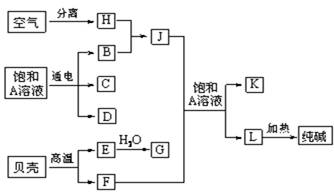
以海水中常见物质A为原料可以发展很多工业生产,如图中包含了中学课本中介绍的几种基本工业生产,请根据如图各物质之间的转化关系回答下列问题.

(1)C和D、C和G反应都可以制取消毒剂.写出C和G反应制取消毒剂的化学反应方程式:
(2)电解A溶液反应的离子方程式为
(3)J分子的空间构型为
(4)实验室可用K与G固体加热制取J,写出该反应化学方程式:

(1)C和D、C和G反应都可以制取消毒剂.写出C和G反应制取消毒剂的化学反应方程式:
2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O
2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O
.(2)电解A溶液反应的离子方程式为
2H2O+2Cl-
Cl2↑+H2↑+2OH-
| ||
2H2O+2Cl-
Cl2↑+H2↑+2OH-
.若该反应中转移电子数为8NA,则产生的氯气在标准状况下体积为
| ||
89.6
89.6
L.(3)J分子的空间构型为
三角锥
三角锥
.(4)实验室可用K与G固体加热制取J,写出该反应化学方程式:
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
.
| ||
分析:由转化关系图可知,A为NaCl,贝壳的主要成分为碳酸钙,则F为CO2,E为CaO,G为Ca(OH)2,H为N2,B为H2,C和D、C和G反应都可以制取消毒剂,则C为Cl2,D为NaOH,J为NH3,J、A、F反应生成L和K,L受热分解生成纯碱,则L为NaHCO3,K为NH4Cl,结合物质的性质来解答.
解答:解:由转化关系图可知,A为NaCl,贝壳的主要成分为碳酸钙,则F为CO2,E为CaO,G为Ca(OH)2,H为N2,B为H2,C和D、C和G反应都可以制取消毒剂,则C为Cl2,D为NaOH,J为NH3,J、A、F反应生成L和K,L受热分解生成纯碱,则L为NaHCO3,K为NH4Cl,
(1)C和G反应制取消毒剂的化学反应方程式为2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(2)电解NaCl溶液的离子反应为2H2O+2Cl-
Cl2↑+H2↑+2OH-,由反应可知,生成22.4L氯气转化2NA电子,则反应中转移电子数为8NA,生成标况下的氯气为22.4L×4=89.6L,
故答案为:2H2O+2Cl-
Cl2↑+H2↑+2OH-;89.6;
(3)J为NH3,空间构型为三角锥型,故答案为:三角锥;
(4)实验室可用K与G固体加热制取J的化学反应为Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O,故答案为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O.
(1)C和G反应制取消毒剂的化学反应方程式为2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(2)电解NaCl溶液的离子反应为2H2O+2Cl-
| ||
故答案为:2H2O+2Cl-
| ||
(3)J为NH3,空间构型为三角锥型,故答案为:三角锥;
(4)实验室可用K与G固体加热制取J的化学反应为Ca(OH)2+2NH4Cl
| ||
| ||
点评:本题考查无机物的推断,明确物质的成分及转化中物质的性质推断出各物质是解答本题的关键,熟悉氯气的性质及氯碱工业等知识即可解答,题目难度中等.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
 以海水中常见物质A为原料可以发展很多工业,图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题.
以海水中常见物质A为原料可以发展很多工业,图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题.