题目内容
【题目】如图所示实验为“套管实验”,小试管内塞有沾有白色无水硫酸铜粉末的棉花球。
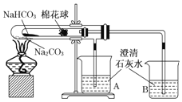
(1)点燃酒精灯加热,能观察到的实验现象是___________________________________。
(2)由上述实验你能得出的结论是_________________________________________。
(3)写出碳酸氢钠受热分解的化学方程式_________________________________________。
【答案】小试管中棉花球变蓝色,B烧杯中澄清石灰水变浑浊,A中有少量气泡冒出 碳酸氢钠受热易分解,有二氧化碳和水生成,碳酸钠受热不分解,无二氧化碳生成,由此可知,碳酸钠的热稳定性比碳酸氢钠强 2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
【解析】
因为NaHCO3的热稳定性不及Na2CO3的热稳定性,所以在加热时大试管中温度高的Na2CO3不分解,小试管中温度低的NaHCO3分解,分解产生的CO2能使B烧杯中的澄清石灰水变浑浊;分解产生的H2O能使棉花球变蓝。
(1)点燃酒精灯加热,大试管中温度高的Na2CO3不分解,小试管中温度低的NaHCO3分解生成碳酸钠、二氧化碳和水,沾有白色无水硫酸铜粉末的棉花球遇H2O生成五水合硫酸铜,使棉花球变蓝;B烧杯中澄清石灰水与二氧化碳反应变浑浊;大试管受热产生的气体不与澄清石灰水反应,可观察到有少量气泡冒出,故答案为:小试管中棉花球变蓝色,B烧杯中澄清石灰水变浑浊,A中有少量气泡冒出;
(2)小试管中为碳酸氢钠,说明温度低时可分解,而碳酸钠受热温度高,碳酸钠不分解,所以该实验说明碳酸氢钠受热易分解,有二氧化碳和水生成,碳酸钠受热不分解,无二氧化碳生成,由此可知,碳酸钠的热稳定性比碳酸氢钠强,故答案为:碳酸氢钠受热易分解,有二氧化碳和水生成,碳酸钠受热不分解,无二氧化碳生成,由此可知,碳酸钠的热稳定性比碳酸氢钠强;
(3)NaHCO3受热分解生成碳酸钠、二氧化碳和水,反应的化学方程式为:2NaHCO3![]() Na2CO3+H2O+CO2↑,故答案为:2NaHCO3
Na2CO3+H2O+CO2↑,故答案为:2NaHCO3![]() Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某同学利用下图装置进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是
X气体 | Y试剂 | Z试剂 | |
A | NO2 | H2O | H2O |
B | HCl | H2O | H2O |
C | HCl和O2混合气体 | H2O | H2O |
D | NH3和N2混合气体 | H2O | H2O |

A. A B. B C. C D. D