题目内容
【题目】50mL0.2mol/L的Na2SO4溶液和50mL0.2mol/L的Al2(SO4)3溶液混合后,溶液中SO42-离子的物质的量浓度为(设混合前后溶液的体积不变)( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】C
【解析】
Na2SO4的物质的量为0.05L×0.2mol/L=0.01mol,则n(SO42)=0.01mol,Al2(SO4)3的物质的量为:0.05mL×0.2mol/L=0.01mol,则n(SO42)=3×0.01mol=0.03mol,所以混合后溶液中(SO42)=0.03mol+0.01mol=0.04mol,混合后溶液的体积可以粗略认为是两溶液混合后体积之和,故硫酸根的物质的量浓度为![]() =0.40mol/L,
=0.40mol/L,
故选C。

练习册系列答案
相关题目
【题目】某原电池结构如图所示,下列有关该原电池的说法不正确的是( )
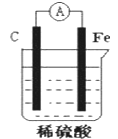
A. 能将化学能转换成电能
B. 电子从碳棒经外电路流向铁棒
C. 碳棒发生还原反应
D. 总反应为Fe+H2SO4= FeSO4+H2↑
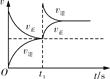
【题目】臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)![]() N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
A | B | C | D |
|
|
|
|
平衡后升温,NO2含量降低 | 0~2 s内,v(O3)=0.2 mol·L-1·s-1 | v正:b点>a点 b点:v逆>v正 | 恒温,t1时再充入O3 |
A. AB. BC. CD. D