题目内容
(7分)(1)某厂废水中含KCN,其浓度为650mg·L-1现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2=KOCN+2KCl+H2O被氧化的元素是_________。
(2)若将等浓度等体积的KCN与HCN混合,测得溶液中c(K+)>c(CN-),则该溶液的pH______7,要使c(K+)=c(CN-),应采取的措施是____________________________.。
(3)若将10m3含KCN的浓度为650mg·L-1的废水中KCN氧化除去,需要标准状况下的氯气的体积为____________L。
(4)已知:
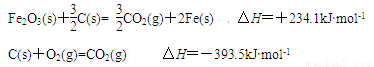
则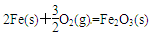 的△H是_________________。
的△H是_________________。
【答案】
(7分)(1)碳(或C);(1分)
(2)(各1分)大于, 加HCN调pH=7即可使c(K+)=c(CN-) (未答pH=7不计分)
(3)5600 (2分) (5)(2分)-824.4kJ·mol-1
【解析】

练习册系列答案
相关题目
Ⅰ.高炉炼铁过程中发生的主要反应为: Fe2O3(s)+CO(g)?
Fe2O3(s)+CO(g)? Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
请回答以下问题:
(1)该反应的平衡常数表达式K=______,△H=______0(填“>”、“<”或“=”).
(2)在体积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡,该时间范围内反应的平均反应速度v(CO2)=______,CO的平衡转化率为______.
Ⅱ.在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质.
(1)某厂废水中含KCN,其浓度为650mg/L.现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2═KOCN+2KCl+H2O,则被氧化的元素是______.
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
______KOCN+______KOH+______Cl2═______CO2+______N2+______KCl+______H2O
(3)若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯______g.
 Fe2O3(s)+CO(g)?
Fe2O3(s)+CO(g)? Fe(s)+CO2(g)
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(1)该反应的平衡常数表达式K=______,△H=______0(填“>”、“<”或“=”).
(2)在体积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡,该时间范围内反应的平均反应速度v(CO2)=______,CO的平衡转化率为______.
Ⅱ.在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质.
(1)某厂废水中含KCN,其浓度为650mg/L.现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2═KOCN+2KCl+H2O,则被氧化的元素是______.
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
______KOCN+______KOH+______Cl2═______CO2+______N2+______KCl+______H2O
(3)若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯______g.