题目内容
25℃时,在某物质的溶液中,由水电离出的c(H+)=1×10-a mol/L,下列说法不正确的是
| A.a<7时,水的电离受到抑制 | B.a>7时,水的电离受到抑制 |
| C.a<7时,溶液的pH可能为a | D.a>7时,溶液的pH可能为14-a |
A
试题分析:a<7时,说明该溶液中水的电离是被促进的,而a>7时,该溶液中水的电离被抑制。酸或碱都是可以抑制水的电离,而盐类的水解可以促进水的电离,所以选项A不正确,其余都是错误的,答案选A。
点评:水是一种弱电解质,存在电离平衡,所以根据水的电离平衡方程式H2O
 H++OH-可以依据勒夏特例原理进行有关判断,其次还需要注意讨论。
H++OH-可以依据勒夏特例原理进行有关判断,其次还需要注意讨论。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 Ba2++2OH-向此种悬浊液中加入少量的氢氧化钡粉末,下列叙述正确的是
Ba2++2OH-向此种悬浊液中加入少量的氢氧化钡粉末,下列叙述正确的是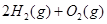 ===
===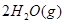
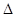 H="-483.6"
H="-483.6" 
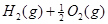 ===
===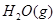
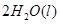
 SO42— + Ca2+
SO42— + Ca2+