题目内容
【题目】现有含Fe(NO3)3、Cu(NO3)2、HNO3的某稀溶液,若向其中逐步加入铁粉,溶液中Fe2+浓度与加入铁粉的物质的量之间的关系如右图所示,则该溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )

A. 1∶1∶3B. 1∶2∶4C. 1∶1∶4D. 1∶3∶1
【答案】C
【解析】
由图可知,加入铁粉后反应先后顺序是:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O、Fe+2Fe(NO3)3=3Fe(NO3)2、Fe+Cu(NO3)2=Fe(NO3)2+Cu;设HNO3、Fe(NO3)3、Cu(NO3)2分别为xmol、ymol、zmol,由于先加入1molFe时没有生成Fe2+,只生成1mol Fe(NO3)3,由系数之比等于物质的量之比可得:n(HNO3)=4n(Fe),则x=4;再加入1molFe时生成3molFe2+,说明参加反应的Fe(NO3)3为2mol,则y=1;最后加入1molFe时生成1mol Fe2+,说明z=1;因此,该溶液中Fe(NO3)3、Cu(NO3)2、HNO3分别为1mol、1mol、4mol,三者的浓度之比为1∶1∶4,故C正确。

【题目】对于下列实验现象的解释,不合理的是
实验 | 现象 | 解释 | |
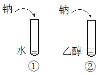
A | | ②中产生气体的速率比①慢 | 乙醇分子中,乙基对羟基产生影响,使O—H键不容易断裂 |
B |
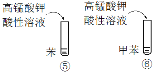
| ③中振荡静置后分层,上层为橙色;④中产生白色沉淀 | 苯酚分子中,苯环对羟基产生影响,使O—H键更容易被取代 |
C |
| ⑤中振荡静置后分层,下层为紫色溶液;⑥中振荡后紫色溶液褪色 | 甲苯分子中,苯环对甲基产生影响,使甲基上C—H更容易被氧化 |
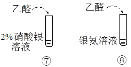
D |
| 水浴加热,⑦中未见明显变化;⑧中试管壁上附着一层光亮的银 | 碱性条件下+1价的Ag才能氧化乙醛 |
A. A B. B C. C D. D
【题目】某无色稀溶液X中,可能含有下表所列离子中的某几种。
阴离子 | CO32-、SiO32-、AlO2-、Cl- |
阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。

(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是________________________,ab段发生反应的离子是________,bc段发生反应的离子方程式为___________________________________。
(2)若Y是NaOH溶液,则X中一定含有的阳离子是____________________, ab段反应的离子方程式为_______________________________________________________________________。