题目内容
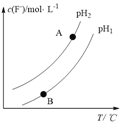
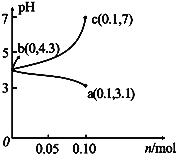
【题目】在25 ℃时,将1.0L c molL-1CH3COOH溶液与0.1molNaOH固体混合,使之充分反应。然后向该混合溶液中加入少量CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述错误的是
A. 水的电离程度:c>b>a
B. a点对应的混合溶液中,c(CH3COOH)>c(Na+ )>c(OH-)
C. 当混合溶液呈中性时,c(Na+ )=c(CH3COO-)>c(H+) =c(OH-)
D. 该温度下,醋酸的电离平衡常数![]()
【答案】D
【解析】A项,由图可得,25℃时c点pH=7,所以c点水电离的c(H+)水=c(OH-)水=10-7mol/L,b点pH=4.3,所以b点溶液中c(H+)=10-4.3 mol/L,则由水电离出的c(H+)水=c(OH-)水=10-(14-4.3)mol/L=10-9.7mol/L,a点pH=3.1,所以a点溶液中c(H+)=10-3.1 mol/L,则由水电离出的c(H+)水=c(OH-)水=10-(14-3.1)mol/L=10-10.9mol/L,因此水的电离程度:c>b>a,故A正确;B项,b点时溶液呈酸性,说明加入0.1molNaOH固体后CH3COOH有剩余,c(Na+)=0.1mol/L,混合前CH3COOH溶液浓度c应比0.1mol/L大,a点时又加入0.1molCH3COOH,因为CH3COOH电离程度很小,所以此时溶液中的c(CH3COOH)一定大于c(Na+),又根据前面的分析a点c(OH-)=10-10.9mol/L,所以a点对应的混合溶液中,c(CH3COOH)>c(Na+)>c(OH-),故B正确;C项,由题意混合溶液中阳离子有Na+和H+,阴离子有CH3COO-和OH-,根据电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),25℃当混合溶液呈中性时,c(H+)=c(OH-)=10-7mol/L,则c(Na+)=c(CH3COO-),由已知及图像可得c(Na+)=0.2mol/L,所以c(Na+)=c(CH3COO-)>c(H+)=c(OH-),故C正确;D项,由前面的分析并结合图像可得,25℃当混合溶液呈中性时,c(H+)=10-7mol/L,c(CH3COO-)=0.2mol/L,c(CH3COOH)=(c+0.1-0.2)mol/L=(c-0.1)mol/L,所以该温度下,醋酸的电离平衡常数Ka=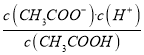 =
=![]() ,故D错误。
,故D错误。