题目内容
15.下列实验操作中有错误的是( )| A. | 1mol任何物质体积的大小取决于构成物质的粒子的大小和粒子之间的距离 | |
| B. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| C. | 蒸馏中,冷却水应从冷凝管的下口通入,上口流出 | |
| D. | 蒸馏时,温度计水银球应浸没在液体中 |
分析 A.由V=nVm可知,一定温度、压强下,体积取决于微粒数,对固体来说,体积取决与粒子的个数及大小、粒子之间的距离;
B.分液时,避免上下层液体混合;
C.蒸馏时,冷水下进上出,在冷凝管中停留时间长;
D.蒸馏时,温度计测定馏分的温度.
解答 解:A.由V=nVm可知,一定温度、压强下,体积取决于微粒数,对固体来说,体积取决与粒子的个数及大小、粒子之间的距离,则1mol任何物质体积的大小取决于构成物质的粒子的大小和粒子之间的距离,故A正确;
B.分液时,避免上下层液体混合,则分液漏斗下层液体从下口放出,上层液体从上口倒出,故B正确;
C.蒸馏时,冷水下进上出,在冷凝管中停留时间长,则冷却水应从冷凝管的下口通入,上口流出,故C正确;
D.蒸馏时,温度计测定馏分的温度,则温度计水银球应在烧瓶的支管口,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯、实验操作为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列化学反应的产物中,存在互为同分异构体的是( )
| A. | CH3CH2CH2Br在碱性溶液中水解 | |
| B. | 甲苯在催化剂FeCl3作用下与Cl2反应 | |
| C. | 3--溴戊烷与NaOH的醇溶液共热反应 | |
| D. |  在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
3.设NA为阿伏伽徳罗常数的值.下列说法正确的是( )
| A. | 1molNa2O2固体中含离子总数为4 NA | |
| B. | 分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g | |
| C. | 28g由C2H4和C3H6组成的混合物中含有氢原子的数目为4NA | |
| D. | 常温下,1mol Fe与过量浓HNO3反应,转移电子的数目为3 NA |
10.一定条件下将0.1mol N2和0.3mol H2置于密闭容器中发生反应:N2+3H2$?_{催化剂}^{高温高压}$2NH3.下列关于该反应的说法正确的是( )
| A. | 最终可生成0.2 mol NH3 | |
| B. | 压缩体积,增大压强能使反应速率减小 | |
| C. | 降低反应体系的温度能加快反应速率 | |
| D. | 容器体积不变,向容器中再加入N2,能加快反应速率 |
20.如图所示,用石墨电极电解CuCl2溶液.下列分析正确的是( )
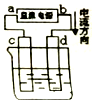

| A. | b为阳极、a为阴极 | |
| B. | 通电一段时间后,d极附近观察到黄绿色气体 | |
| C. | 阳极上发生的反应:Cu2++2e-═Cu | |
| D. | 若电路中转移0.2mole-,则d极增重6.4g |
 在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题. .
.
