��Ŀ����
14����KMnO4�����ܶ�Ϊ1.19g/cm3��������������Ϊ36.5%��������Һ����Ӧ����ʽ���£�2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O��1��HCl��Һ�����ʵ���Ũ�ȣ�
��2��15.8g KMnO4��ʹ���ٿ�HCl����������Ӧ���ж��ٿ�HCl��������
��3����Cl2�ڱ�״���µ��ܶ�Ϊ3.17g/L���������Cl2�ڱ�״���µ����Ϊ���٣�
���� ��1������c=$\frac{1000�Ѧ�}{M}$������������ʵ���Ũ�ȣ�
��2������n=$\frac{m}{M}$����KMnO4�����ʵ��������ݷ���ʽ����μӷ�Ӧ��HCl����������HCl����������������ԭ���Ǽ��㱻����HCl���ʵ�����
��3������V=nVm�������������������
��� �⣺��1����c=$\frac{1000�Ѧ�}{M}$��֪���ܶ�Ϊ1.19g/cm3��������������Ϊ36.5%����������ʵ���Ũ��Ϊ$\frac{1000��1.19��36.5%}{36.5}$mol/L=11.9mol/L��
�𣺸���������ʵ���Ũ��Ϊ11.9mol/L��
��2��15.8g KMnO4�����ʵ���Ϊ$\frac{15.8g}{158g/mol}$=0.1mol������2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O����֪�μӷ�Ӧ��HClΪn��HCl��=8n��KMnO4��=0.8mol����m��HCl��=0.8mol��36.5g/mol=29.2g��
n��Cl2��=$\frac{5}{2}$n��KMnO4��=0.1mol��$\frac{5}{2}$=0.25mol����������HCl����������������ԭ�ӿ�֪��������HCl���ʵ���Ϊ0.25mol��2=0.5mol�����Ա�����HCl������Ϊ0.5mol��36.5g/mol=18.25g��
��15.8g KMnO4��ʹ29.2��HCl����������Ӧ��18.25��HCl��������
��3���ڱ�����������������Ϊ0.25mol��22.4L/mol=5.6L��
��Cl2�ڱ�״���µ����Ϊ5.6L��
���� ���⿼�����ʵ���Ũ�ȼ��㡢��ѧ����ʽ���㣬�ѶȲ���ע��Ի���֪ʶ���������գ�

 ����������ϵ�д�
����������ϵ�д� ��ͼ��ʵ�������Ҵ���Ũ������廯�Ʒ�Ӧ���Ʊ��������װ�ã���Ӧ��Ҫ���ȣ�ͼ��ʡȥ�˼���װ�ã��й����ݼ��±���
��ͼ��ʵ�������Ҵ���Ũ������廯�Ʒ�Ӧ���Ʊ��������װ�ã���Ӧ��Ҫ���ȣ�ͼ��ʡȥ�˼���װ�ã��й����ݼ��±����Ҵ��������顢���йز�����
| �Ҵ� | ������ | �� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | �����ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 1.44 | 3.1 |
| �е�/�� | 78.5 | 38.4 | 59 |
a�����ٸ�����ϩ���ѵ����� b������Br2������ c������HBr�Ļӷ� d��ˮ�Ƿ�Ӧ�Ĵ���
��2����֪�����¶Ƚϵ�ʱNaBr�����ᷴӦ����NaHSO4��д������ʱA�з�������Ҫ��Ӧ�Ļ�ѧ����ʽCH3CH2OH+NaBr+H2SO4$\stackrel{��}{��}$NaHSO4+CH3CH2Br+H2O��
��3������B���������������ܣ���ȴˮӦ��B���£���ϡ����¡�����������
��4����Ӧ���ɵ�������Ӧ��C�У��A����C���У���
��5������Ũ���������ʵ��ʱ���õ�����������ػ�ɫ�����ѡ������c��ѡ����ţ���Һ��ϴ�Ӳ�Ʒ��
a���������� b���������� c���⻯���� d��̼������
ϴ�Ӳ�Ʒʱ����Ҫ�IJ��������з�Һ©�����ձ���
| A�� | ��һ��ǿ��ͨ��������Һ��Ҳ�ܲ��������ЧӦ | |
| B�� | ������1 mol Fe��OH��3�Ľ����У�Լ��6.02��1023��Fe��OH��3���� | |
| C�� | һ֦�ֱ�ʹ�����ֲ�ͬ�ͺŵ�����īˮ���׳��ֶ��� | |
| D�� | �����ʺ硱��������¥������һ����Ȼ�������ǹ�ѧ����Ҳ�뽺��������й� |
��1��������裺��������м��貹��������
����1���ù���������FeCl2��
����2���ù���������FeCl3��
����3���ù���������FeCl3��FeCl2��
��2�����ʵ�鷽����
ȡ������������A���ձ��У�������ˮ�ܽ�A��Ȼ��ȡ����A��Һ�ֱ����ʵ�飬ʵ��������������±��������ڱ���ĺ��ߴ���գ�
| ʵ�鷽�� | ʵ������ | ���� |
| ����Һ�м���KSCN��Һ | ��Һ���ɫ | ������������FeCl3 |
| ������KMnO4��Һ�м�������A | KMnO4��Һ��ɫ�����Ա仯 | ���������в���FeCl2 |
��4��ȡ100mL0.2mol/L��FeCl3��Һ�����ձ��У������м���һ������Fe��Cu������ַ�Ӧ�����й���ʣ�࣬��������һ����ȷ����CD������Һ������䣬������ˮ�����أ���
A���ձ�����Fe��Cu��c��Fe2+��=0.2mol/L B���ձ�����Cu��Fe��c��Fe2+��=0.3mol/L
C���ձ�����Cu��Fe��c��Cl-��=0.6mol/L D���ձ���Fe��Cu���У�c��Fe2+��=0.3mol/L
��5����FeSO4����Һ�м�����FeSO4�����ʵ�����Na2O2���壬ǡ��ʹFeSO4ת��ΪFe��OH��3��д���÷�Ӧ�����ӷ���ʽ4Fe2++4Na2O2+6H2O=4Fe��OH��3��+O2��+8Na+��
| A�� | C3H8 | B�� | C7H8O | C�� | CH4O | D�� | CH2Cl2 |
ѧϰС���ڽ���1-�ȱ�����NaOH�Ҵ���Һ�ķ�Ӧ�У��۲쵽���������ɣ�
����������ֲ�ͬ�ķ����ֱ��������壮�ڴ���ķ�����д��װ������ʢ�Լ������ƣ��Լ���ѡ����ʵ������
| װ��ͼ | ��ʢ�Լ� | ʵ������ | |
| 1 | 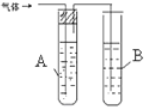 | A�� ˮ B�� ���Ը��������Һ | |
| 2 | 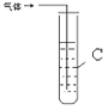 | C�� ������Ȼ�̼��Һ |
 ����д���÷�Ӧ��һ����Ҫ��;�����Ӹֹ죮
����д���÷�Ӧ��һ����Ҫ��;�����Ӹֹ죮