题目内容
下列各项表述与示意图一致的是( )

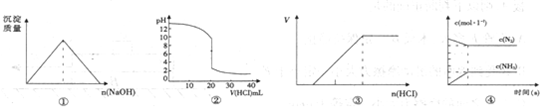
分析:A、向AlCl3溶液中滴入NaOH溶液,先发生反应Al3+3OH-=Al(OH)3,先生成沉淀,铝离子反应完毕,发生反应Al(OH)3+OH-=AlO2-+H2O,沉淀溶解,前后氢氧化钠的物质的量为3:1.
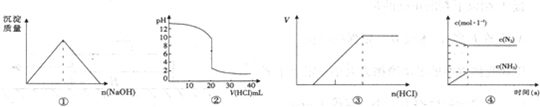
B、0.01mol?L-1NaOH溶液PH=12,随加入酸体积的变化,溶液PH值降低,20mL0.01mol?L-1NaOH溶液完全反应需要盐酸20mL.
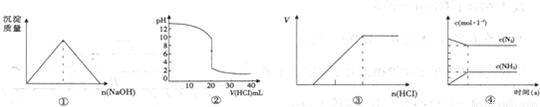
C、向Na2CO3稀溶液中滴入稀HCl,先发生反应CO32-+H+=HCO3-,不产生二氧化碳,碳酸钠反应完毕,发生反应H++HCO3-=CO2↑+H2O,前后盐酸的体积比为1:1.
D、该反应为可逆反应,随反应进行,氮气的浓度降低,氨气的浓度增大,二者浓度变化为1:2.
B、0.01mol?L-1NaOH溶液PH=12,随加入酸体积的变化,溶液PH值降低,20mL0.01mol?L-1NaOH溶液完全反应需要盐酸20mL.
C、向Na2CO3稀溶液中滴入稀HCl,先发生反应CO32-+H+=HCO3-,不产生二氧化碳,碳酸钠反应完毕,发生反应H++HCO3-=CO2↑+H2O,前后盐酸的体积比为1:1.
D、该反应为可逆反应,随反应进行,氮气的浓度降低,氨气的浓度增大,二者浓度变化为1:2.
解答:解:A、向AlCl3溶液中滴入NaOH溶液,先发生反应Al3+3OH-=Al(OH)3,先生成沉淀,铝离子反应完毕,发生反应Al(OH)3+OH-=AlO2-+H2O,沉淀溶解,前后氢氧化钠的物质的量为3:1,图①中沉淀生成与沉淀溶解,消耗的氢氧化钠的物质的量为1:1,不符合3:1,故A错误;
B、0.01mol?L-1NaOH溶液PH=12,随加入酸体积的变化,溶液PH值降低,20mL0.01mol?L-1NaOH溶液完全反应需要盐酸20mL,图②中氢氧化钠的起始PH大于12,故B错误;
C、向Na2CO3稀溶液中滴入稀HCl,先发生反应CO32-+H+=HCO3-,不产生二氧化碳,碳酸钠反应完毕,发生反应H++HCO3-=CO2↑+H2O,前后盐酸的体积比为1:1,图③中前后两过程消耗的盐酸为1:2,不是1:1,与实际不符,故C错误;
D、该反应为可逆反应,随反应进行,氮气的浓度降低,氨气的浓度增大,二者浓度变化为1:2,图④与实际相符合,故D正确.
故选:D.
B、0.01mol?L-1NaOH溶液PH=12,随加入酸体积的变化,溶液PH值降低,20mL0.01mol?L-1NaOH溶液完全反应需要盐酸20mL,图②中氢氧化钠的起始PH大于12,故B错误;
C、向Na2CO3稀溶液中滴入稀HCl,先发生反应CO32-+H+=HCO3-,不产生二氧化碳,碳酸钠反应完毕,发生反应H++HCO3-=CO2↑+H2O,前后盐酸的体积比为1:1,图③中前后两过程消耗的盐酸为1:2,不是1:1,与实际不符,故C错误;
D、该反应为可逆反应,随反应进行,氮气的浓度降低,氨气的浓度增大,二者浓度变化为1:2,图④与实际相符合,故D正确.
故选:D.
点评:考查图象分析,涉及铝化合物性质、碳酸盐性质、中和滴定、可逆反应等,难度中等,清楚反应过程与可逆反应的特点是关键,注意图象中量的关系.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
下列各项表述与示意图一致的是( )
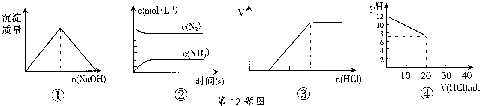
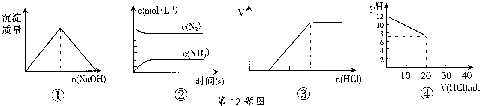
| A、图①表示向AlCl3溶液中滴入NaOH溶液,沉淀质量的变化 | B、图②表示合成氨反应,N2和NH3的物质的量浓度随反应时间的变化关系 | C、图③表示向Na2CO3稀溶液中滴入稀盐酸,产生气体的体积随加入盐酸的变化关系 | D、图④表示室温时,用0.01mol?L-1 HCl溶液滴定20mL 0.01mol?L-1 NaOH溶液,溶液的pH随加入盐酸体积的变化关系 |