题目内容
完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写:(1)已知:2Cu(s)+
 O2(g)=Cu2O(s);△H=-169kJ?mol-1,
O2(g)=Cu2O(s);△H=-169kJ?mol-1,C(s)+
 O2(g)=CO(g);△H=-110.5kJ?mol-1,
O2(g)=CO(g);△H=-110.5kJ?mol-1,Cu(s)+
 O2(g)=CuO(s);△H=-157kJ?mol-1
O2(g)=CuO(s);△H=-157kJ?mol-1用炭粉在高温条件下还原CuO生成Cu2O的热化学方程式是:______
(2)在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g),写出该反应的化学平衡常数表达式:______
(3)以甲烷、空气为反应物,KOH溶液作电解质溶液构成燃料电池,则负极反应式为:______.
(4)无水AlCl3瓶盖打开有白雾,其反应的化学方程式为______.
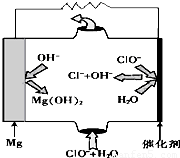
(5)“镁-次氯酸盐”燃料电池,其装置示意图如图,该电池反应的总反应方程式为______.
(6)工业上电解饱和食盐水的离子方程式为______ 2OHˉ+Cl2↑+H2↑
(2)平衡常数指生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值.
(3)原电池负极发生氧化反应,甲烷在负极放电,氧气在正极反应,碱性条件下氧气放电生成氢氧根离子,正极电极反应式为2O2+4H2O+8e-=8OH-,总的电池反应式为CH4+2O2+2OHˉ=CO32ˉ+3H2O,电池总反应式减去正极电极反应式可得负极电极反应式.
(4)AlCl3水解产生HCl,氯化氢与空气中的水蒸气呈白雾.
(5)由图可知镁-次氯酸盐”燃料电池中Mg与ClO-、H2O反应生成Cl-与Mg(OH)2.
(6)电解饱和食盐水生成氯气、氢气、氢氧化钠.
解答:解:(1)已知:①2Cu(s)+
 O2(g)=Cu2O(s);△H=-169kJ?mol-1,
O2(g)=Cu2O(s);△H=-169kJ?mol-1,②C(s)+
 O2(g)=CO(g);△H=-110.5kJ?mol-1,
O2(g)=CO(g);△H=-110.5kJ?mol-1,③Cu(s)+
 O2(g)=CuO(s);△H=-157kJ?mol-1
O2(g)=CuO(s);△H=-157kJ?mol-1=-169kJ?mol-1,
由盖斯定律可知,①-③×2+②得2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=-169kJ?mol-1-(-157kJ?mol-1)×2+(-110.5kJ?mol-1)=+34.5 kJ?mol-1.
故答案为:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=+34.5 kJ?mol-1.
(2)可逆反应2SO2(g)+O2(g)?2SO3(g)的化学平衡常数k=
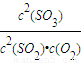 .
.故答案为:
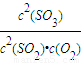 .
.(3)原电池负极发生氧化反应,甲烷在负极放电,氧气在正极反应,碱性条件下氧气放电生成氢氧根离子,正极电极反应式为2O2+4H2O+8e-=8OH-,总的电池反应式为CH4+2O2+2OHˉ=CO32ˉ+3H2O,电池总反应式减去正极电极反应式可得负极电极反应式为CH4+10OHˉ-8eˉ=CO32ˉ+7H2O.
故答案为:CH4+10OHˉ-8eˉ=CO32ˉ+7H2O.
(4)AlCl3水解AlCl3+3H2O
故答案为:AlCl3+3H2O
(5)由图可知镁-次氯酸盐”燃料电池中Mg与ClO-、H2O反应生成Cl-与Mg(OH)2,该电池反应的总反应方程式为
Mg+ClO-+H2O=Cl-+Mg(OH)2.
故答案为:Mg+ClO-+H2O=Cl-+Mg(OH)2.
(6)电解饱和食盐水生成氯气、氢气、氢氧化钠,电解饱和食盐水的离子方程式为2Clˉ+2H2O
 2OHˉ+Cl2↑+H2↑.
2OHˉ+Cl2↑+H2↑.故答案为:2Clˉ+2H2O
 2OHˉ+Cl2↑+H2↑.
2OHˉ+Cl2↑+H2↑.点评:考查盖斯定律与热化学方程式书写、化学平衡常数、原电池、盐类水解、电解池等,综合性较大,难度中等,是对知识的综合运用,注意基础知识的理解掌握.

(4分)已知25℃、101kpa时,一些物质的燃烧热为:
| 化学式 | CO(g) | H2(g) | CH3OH(l) |
| △H/(KJ/mol) | -283.0 | -285.8 | -726.5 |
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式: 。
(2)根据盖斯定律完成下列热化学方程式 CO(g)+ 2H2(g)= CH3OH(l) △H=
(4分)已知25℃、101kpa时,一些物质的燃烧热为:
| 化学式 | CO(g) | H2(g) | CH3OH(l) |
| △H/(KJ/mol) | -283.0 | -285.8 | -726.5 |
(2)根据盖斯定律完成下列热化学方程式CO(g)+ 2H2(g)= CH3OH(l) △H=
完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写:
(1)已知:2Cu(s)+1/2O2(g)=Cu2O(s);△H=-169kJ·mol-1,
C(s)+1/2O2(g)=CO(g);△H=-110.5kJ·mol-1,
Cu(s)+1/2O2(g)=CuO(s);△H=-157kJ·mol-1
用炭粉在高温条件下还原CuO生成Cu2O的热化学方程式是:
(2)在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) 2SO3(g),写出该反应的化学平衡常数表达式:
2SO3(g),写出该反应的化学平衡常数表达式:
(3)以甲烷、空气为反应物,KOH溶液作电解质溶液构成燃料电池,则负极反应式为: 。
(4)铁在潮湿的空气中发生吸氧腐蚀的电池反应方程式为 。
(5)“镁—次氯酸盐”燃料电池,其装置示意图如图,该电池反应的总反应方程式为_______________ 。
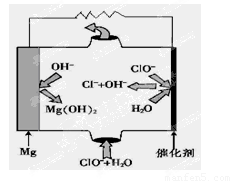
(6)工业上电解熔融氯化钠的方程式为 。
(4分)已知25℃、101kpa时,一些物质的燃烧热为:
|
化学式 |
CO(g) |
H2(g) |
CH3OH(l) |
|
△H/(KJ/mol) |
-283.0 |
-285.8 |
-726.5 |
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式: 。
(2)根据盖斯定律完成下列热化学方程式 CO(g)+ 2H2(g)= CH3OH(l) △H=
 完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写:
完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写: Al(OH)3+3HCl
Al(OH)3+3HCl