��Ŀ����
����Ŀ��ʵ��������ƿʧȥ��ǩ����ɫ��Һ���Ȼ��ء��������ƺ�ϡ���ᣬ����һ�ֳ������ָʾ��X ��Na2CO3һ�μ������ǣ������йز����������Լ���գ� 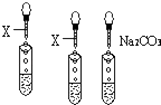
��1��������Һ����ɫ����ȡ����Һ����Na2CO3��Һ�У��������������ƶ��Լ�XΪ ��
��2��������Һ����ɫ����ȡ����Һ����Na2CO3��Һ�е�����Ϊ �� �йط�Ӧ�����ӷ���ʽΪ ��
��3�����������ݲ������йط�Ӧ�����ӷ���ʽΪ����ȡ����Һ�����Լ�X������Һ�� ��
���𰸡�
��1����ɫʯ����Һ
��2���а�ɫ����������CO32��+Ca2+�TCaCO3��
��3��CO32��+2H+�TH2O+CO2 ������ɫ
���������⣺��1���Ȼ��ء��������ƺ�ϡ����������Һ�У���Һ����ɫ��˵���μ�ʯ�ӦΪ������ҺKCl��ʯ����Һ����ɫ����̼���Ʋ���Ӧ�� ���Դ��ǣ���ɫʯ����Һ����2��������Һ����������ʹ��ɫʯ����Һ����ɫ�������������ƺ�Na2CO3��Һ��Ӧ����̼��Ƴ������������ƣ�ʵ���ǣ�CO32��+Ca2+�TCaCO3����
���Դ��ǣ��а�ɫ����������CO32��+Ca2+�TCaCO3������3��������һ���ᣬ��ʯ����Һ�Ժ�ɫ�����������У�ֻ�������ܺ�̼���Ʒ�Ӧ�����Ȼ��ơ�ˮ��������̼����Ӧ�����ӷ���ʽΪCO32��+2H+�TH2O+CO2 ����
���Դ��ǣ�CO32��+2H+�TH2O+CO2 ������ɫ��

����Ŀ���±���ij���ӵ�ʳ�Ρ���װ���ϵIJ�������˵����
���� | �Ȼ��ƣ�NaCl��������أ�KIO3�� |
������ | 20��40mgkg��1 |
������ | 18���� |
ʳ�÷��� | ��ʱ������ |
����ָ�� | ���ȡ��ܹ⡢�ܷ⡢���� |
��1�����ⶨ���á��ӵ�ʳ�Ρ���KIO3�ĺ���Ϊ42.8mgkg��1 �� ����ÿǧ�ˡ��ӵ�ʳ�Ρ���KIO3�����ʵ���Ϊ���٣��á��ӵ�ʳ�Ρ��ĺ�����Ϊ���٣���
��2����5.0g�á��ӵ�ʳ�Ρ�����ˮ�����100mL��Һ������Һ��IO ![]() �������ʵ���Ũ��Ϊ���٣�
�������ʵ���Ũ��Ϊ���٣�
