题目内容
下列离子方程式书写正确的是 ( )
| A.氢氧化钡与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| B.Al2O3溶于盐酸中:O2-+2H+=H2O |
| C.氯化铝溶液中加入少量氨水:Al3+ + 3OH-= Al(OH)3↓ |
D.氯气与水反应 Cl2+H2O H+ + Cl-+ HClO H+ + Cl-+ HClO |
D
解析试题解析:A、氢氧化钡与稀硫酸反应除有沉淀生成外还有水生成,错误;B、Al2O3属于氧化物不可拆,错误;C、氨水中的一水合氨属于弱碱,不可写成OH-,错误;D、氯气和水反应生成的HClO属于弱酸,不可拆,正确,答案选D。
考点:考查离子方程式书写的相关知识

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
微粒甲与离子乙在溶液中的转化关系如图所示: 甲是
甲是
| A.Si | B.NH4+ | C.Al | D.SO2 |
下列说法错误的是
| A.除去MgCl2溶液中少量的FeCl3,可选用MgCO3 |
| B.稀硫酸中加入Zn粉,随着反应的进行,溶液中水的电离程度逐渐增大 |
| C.能溶解氧化铝的溶液中可能大量存在:HCO3-、SO42-、NO3-、Na+ |
| D.等物质的量浓度的(NH4)2SO4溶液和(NH4)2CO3溶液中NH4+浓度前者大于后者 |
向含等物质的量两种溶质的甲溶液中逐渐加入乙物质,生成不溶物的量(Y)与加入物的量(X)之间的关系符合如图所示的是
| | 甲溶液 | 乙物质 |
| A | HCl和CaCl2 | NaHCO3溶液 |
| B | H2SO4和MgSO4 | NaOH溶液 |
| C | Fe2(SO4)3和CuSO4 | Fe粉 |
| D | AlCl3和HCl | NH3气体 |
下列反应的离子方程式,书写正确的是
A.钠跟水反应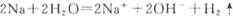 |
B.溶液中加入过量氨水 |
C.硫酸和氢氧化钡溶液反应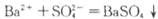 |
D.大理石跟盐酸反应放出气体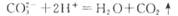 |
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。则原溶液中Al3+、Mg2+、NH4+的物质的量分别为 ( )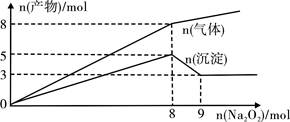
| A.2 mol、3 mol、8 mol |
| B.3 mol、2 mol、8 mol |
| C.2 mol、3 mol、4 mol |
| D.3 mol、2 mol、4 mol |
能正确表示下列反应的离子方程式的为( )
A.硫化亚铁溶于稀硝酸中:FeS+2H+ Fe2++H2S↑ Fe2++H2S↑ |
B.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O Al Al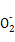 +4N +4N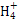 +2H2O +2H2O |
C.硫代硫酸钠溶液中滴入稀盐酸:S2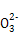 +2H+ +2H+ S↓+SO2↑+H2O S↓+SO2↑+H2O |
D.在NaHSO4溶液中滴加Ba(OH)2至中性:H++S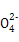 +Ba2++OH- +Ba2++OH- BaSO4↓+H2O BaSO4↓+H2O |
下列对各组离子或物质是否能够大量共存解释正确的是( )。
| A | 常温常压下NH3、O2、H2、CO2 | 不能共存 | NH3为碱性气体、CO2为酸性气体,二者反应生成(NH4)2CO3 |
| B | c(OH-)=1.0×10-13 mol·L-1溶液中,Fe2+、NO3—、SO42—、Na+ | 不能共存 | 发生反应:3Fe2++NO3—+4H+=3Fe3++NO↑+2H2O |
| C | 溶液中:K+、Cu2+、Cl-、NH3·H2O | 不能共存 | 发生反应:Cu2++2OH-=Cu(OH)2↓ |
| D | 溶液中:Al3+、Na+、SO42—、HCO3— | 可以共存 | 不能发生反应 |
下列表示对应化学反应的离子方程式正确的是 ( )。
| A.向AlCl3溶液中加入过量浓氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| B.将含有0.1 mol Ba(OH)2的溶液与含有0.2 mol NaHSO4的溶液混合:H++SO42-+OH-+Ba2+=BaSO4↓+H2O |
| C.向澄清石灰水中通入过量CO2:OH-+CO2=HCO3- |
| D.Na2O2溶于水:2O2-+2H2O=4OH-+O2↑ |