��Ŀ����
����Ŀ�����ǻ�ѧʵ���Ҽ����������е���Ҫ���ʣ�Ӧ�ù㷺��
��1����֪25��ʱ��N2��g��+O2��g��![]() 2NO��g�� ��H1��+183 kJ��mol
2NO��g�� ��H1��+183 kJ��mol
2H2��g��+O2��g����2H2O��l�� ��H2��-571.6 kJ��mol
4NH3��g��+5O2��g����4NO��g��+6H2O��1�� ��H3��-1164.4 kJ��mol
��N2��g��+3H2��g��![]() 2NH3��g�� ��H��________kJ��mol
2NH3��g�� ��H��________kJ��mol
N2 | H2 | NH3 | |
Ͷ��I | 1.0 mol/L | 3.0 mol/L | 0 |
Ͷ��II | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
��2���ں��º����ܱ������н��кϳɰ���Ӧ����ʼͶ��ʱ������Ũ�����±���
�ٸ��¶��ºϳɰ���Ӧ��ƽ�ⳣ������ʽΪ________��
�ڰ�Ͷ��I���з�Ӧ����ôﵽ��ѧƽ��״̬ʱH2��ת����Ϊ40��������Ͷ��II���з�Ӧ����ʼʱ��Ӧ���еķ���Ϊ________�������������
���������¶ȣ���ϳɰ���Ӧ�Ļ�ѧƽ�ⳣ��___________����������С�����䡱����
��L��L1��L2����X�ɷֱ����ѹǿ���¶ȡ���ͼ��ʾLһ��ʱ���ϳɰ���Ӧ��H2��g����ƽ��ת������X�ı仯��ϵ��

i X��������������_________��
ii �ж�L1��L2�Ĵ�С��ϵ�����������ɣ�_____________��
��3����ͼ��һ���õ��ԭ�����Ʊ�H2O2�����ò�����H2O2�����ϰ�ˮ��װ�á�

Ir-Ru���Ե缫����O2����H2O2����缫��Ӧʽ��__________��
���𰸡� -92.2 K��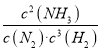 ���� ��С �¶� L1<L2�����¶�һ��ʱ��ѹǿԽ��ƽ��ת����Խ�� O2+2H++2e-��H2O2
���� ��С �¶� L1<L2�����¶�һ��ʱ��ѹǿԽ��ƽ��ת����Խ�� O2+2H++2e-��H2O2
��������(1)��֪25��ʱ����N2(g)+O2(g) ![]() 2NO(g)��H=+183kJ/mol����2H2(g)+O2(g)
2NO(g)��H=+183kJ/mol����2H2(g)+O2(g) ![]() 2H2O(l)��H=-571.6kJ/mol����4NH3(g)+5O2(g)
2H2O(l)��H=-571.6kJ/mol����4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(l)��H=-1164.4kJ/mol�����ݸ�˹���ɢ�+����
4NO(g)+6H2O(l)��H=-1164.4kJ/mol�����ݸ�˹���ɢ�+����![]() -
-![]() ���۵ã�N2(g)+3H2(g)
���۵ã�N2(g)+3H2(g) ![]() 3NH3(g)��H=+183-571.6��
3NH3(g)��H=+183-571.6��![]() -
-![]() ��1164.4=-92.2kJ/mol���ʴ�Ϊ��-92.2��
��1164.4=-92.2kJ/mol���ʴ�Ϊ��-92.2��
(2)����Ϊ�ϳɰ���Ӧ��ƽ�ⳣ��=������Ũ�ȵ��ݴη�֮�����Ϸ�Ӧ��Ũ�ȵ��ݴη�֮��������N2(g)+3H2(g) ![]() 3NH3(g)��ƽ�ⳣ������ʽΪK=
3NH3(g)��ƽ�ⳣ������ʽΪK=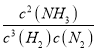 ���ʴ�Ϊ��K=
���ʴ�Ϊ��K=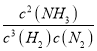 ��
��
�ڰ�Ͷ�Ϣ�����ȫת�����ұߣ�����Ͷ�Ϣ���ȫ��ͬ��Ϊ��ȫ��Чƽ�⣬����Ͷ�Ϣ���з�Ӧƽ��ʱH2��Ũ��ҲΪ3.0mol/L��(1-40%)=1.8mol/L������Ͷ�Ϣ���з�Ӧ����ʼʱ��Ӧ���淴Ӧ������У��ʴ�Ϊ������
����(1)�ó��ϳɰ�Ϊ���ȷ�Ӧ�����������¶�ƽ�����淴Ӧ�����ƶ������Է�Ӧ�Ļ�ѧƽ�ⳣ����С���ʴ�Ϊ����С��
��i����ͼ��֪��XԽ������ת����Խ�ͣ������¶�ƽ�����淴Ӧ�����ƶ���������ת���ʼ�С����X��ʾ�¶ȣ��ʴ�Ϊ���¶ȣ�
ii����N2(g)+3H2(g)3NH3(g)��H��0���¶ȸߣ�����ת����С��ѹǿ��ƽ�������ƶ�������ת���ʴ�ͼ����ͬ�¶�ʱL2��Ӧ������ת���ʴ���ѹǿL1��L2���ʴ�Ϊ��L1��L2�����¶�һ��ʱ��ѹǿԽ��ƽ��ת����Խ����
�����õ�ⷨ��H2O2���ڸõ����У�Ir-Ru���Ե缫������O2����Ϊ�����õ��ӷ�����ԭ��Ӧ��O2+2H++2e-�TH2O2���ʴ�Ϊ��O2+2H++2e-=H2O2��

