题目内容
【题目】元素M的最高正价和负价的绝对值之差为6,M、N的离子具有相同的电子排布,则M、N所形成的化合物可能是( )
A.MgF2 B.MgCl2 C.CaCl2 D.CaBr2
【答案】C
【解析】
试题分析:元素M的最高正价和负价的绝对值之差为6,则M位于第ⅦA族,M、N的离子具有相同的电子排布,则N在M的下一周期,原子的最外层有一个会两个电子。由于F无最高正价,选项A排除,Mg和Cl及Ca和Br都是同一周期的元素,不符合题意,所以选项B、D排除。根据选项提供的物质可知M、N所形成的化合物可能是CaCl2,因此选项是C。

练习册系列答案
相关题目
【题目】纯净物根据其组成和性质可进行如下分类。
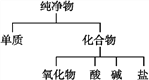
(1)如图所示的分类方法属于______(填字母)。
A.交叉分类法 B.树状分类法
(2)以H、O、S、N、K、Ca六种元素中任意两种或三种元素组成合适的常见物质,分别将其中一种常见物质的化学式填在下表相应类别中:
物质类别 | 酸 | 碱 | 盐 | 氧化物 |
化学式 |
_______________、_________________、______________________、__________________;
(3)从上表中选出一种酸和一种氧化物,写出其反应的化学方程式:________________。