题目内容
(2011?临沂模拟)A、B、C、D、E均是由下列离子组成的可溶性化合物.组成这五种物质的离子有(离子不能重复组合):
分别取它们进行实验,结果如下:
①A溶液与D溶液混合,没有明显现象;
②当B溶液加入到D溶液中时,有沉淀产生.继续加入B溶液,沉淀全部消失.
③将E溶液加热,有沉淀生成.
据此推断:A
| 阳离子 | Na+ Mg2+ Al3+ Ba2+ Fe3+ | ||||||
| 阴离子 | OH- Cl- CO
|
①A溶液与D溶液混合,没有明显现象;
②当B溶液加入到D溶液中时,有沉淀产生.继续加入B溶液,沉淀全部消失.
③将E溶液加热,有沉淀生成.
据此推断:A
Fe2(SO4)3
Fe2(SO4)3
;BBa(OH)2
Ba(OH)2
;CNa2CO3
Na2CO3
;DAlCl3
AlCl3
;EMg(HCO3)2
Mg(HCO3)2
.分析:该题抓住“可溶性化合物”说明五种物质均溶于水进行分析,根据当B溶液加入到D溶液中时,有沉淀产生,继续加入B溶液,沉淀全部消失,可推测是铝盐与强碱溶液反应的特征现象,根据碳酸根离子只能与阳离子钠离子结合形成可溶性的盐,所以强碱溶液B只能为氢氧化钡;再根据E加热生成沉淀推断出E为碳酸氢镁;再根据A溶液与D氯化铝溶液混合,没有明显现象推断出A,据此完成即可.
解答:解:A、B、C、D、E均是由下列离子组成的可溶性化合物,根据当B溶液加入到D溶液中时,有沉淀产生,继续加入B溶液,沉淀全部消失,可推测是铝盐与强碱溶液反应的特征现象,B为强碱溶液;由于CO3 2-形成的可溶性盐只有Na2CO3,则强碱只有Ba(OH)2;由②知B为Ba(OH)2,D只能为AlCl3;
③将E溶液加热,有沉淀生成,可知E只能为Mg(HCO3)2;
再由①知A为Fe2(SO4)3;则C为Na2CO3,
所以A为:Fe2(SO4)3、B为:Ba(OH)2、C:为Na2CO3、D为:AlCl3、E为:Mg(HCO3)2,
故答案为:Fe2(SO4)3;Ba(OH)2;Na2CO3;AlCl3;Mg(HCO3)2.
③将E溶液加热,有沉淀生成,可知E只能为Mg(HCO3)2;
再由①知A为Fe2(SO4)3;则C为Na2CO3,
所以A为:Fe2(SO4)3、B为:Ba(OH)2、C:为Na2CO3、D为:AlCl3、E为:Mg(HCO3)2,
故答案为:Fe2(SO4)3;Ba(OH)2;Na2CO3;AlCl3;Mg(HCO3)2.
点评:本题考查了常见离子的检验方法,题目难度不大,注意抓住“可溶性化合物”说明五种物质均溶于水进行分析,本题充分考查了学生的分析、理解能力,要求熟练掌握常见离子的检验方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
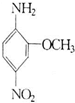 (2011?临沂模拟)2一氨基一5一硝基苯甲醚俗称红色基B,主要用于棉纤维织物的染色,也用于制金黄、枣红、黑等有机颜料,其结构简式如右所示.若分子式与红色基B相同,且氨基(-NH2)与硝基(-NO2)直接连在苯环上并呈对位时的同分异构体数目(包括红色基B)可能为( )
(2011?临沂模拟)2一氨基一5一硝基苯甲醚俗称红色基B,主要用于棉纤维织物的染色,也用于制金黄、枣红、黑等有机颜料,其结构简式如右所示.若分子式与红色基B相同,且氨基(-NH2)与硝基(-NO2)直接连在苯环上并呈对位时的同分异构体数目(包括红色基B)可能为( )