题目内容
根据元素周期律和元素周期表的知识分析下面的推断,其中错误的是( )
| A、铍(Be)的氧化物及氢氧化物可能具有两性 |
| B、砹(At)的单质是有色固体,HAt很不稳定 |
| C、H2Se是无色、有毒的气体 |
| D、Sr(OH)2的碱性强于Ba(OH)2 |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.Be与Al在周期表中位于对角线位置,性质相似;
B.由卤族元素单质及化合物的递变性分析;
C.同主族元素单质及其化合物的性质相似;
D.同主族从上到下金属增强,金属性越强,对应最高价氧化物的水化物的碱性越强.
B.由卤族元素单质及化合物的递变性分析;
C.同主族元素单质及其化合物的性质相似;
D.同主族从上到下金属增强,金属性越强,对应最高价氧化物的水化物的碱性越强.
解答:
解:A.Be与Al在周期表中位于对角线位置,性质相似,氢氧化铝具有两性,则铍(Be)是一种金属,它的最高价氧化物的水化物可能具有两性,故A正确;
B.由卤族元素单质及化合物的递变性可知,单质的颜色随原子序数增大加深,气态氢化物稳定性减弱,则砹是一种有色固体,HAt不稳定,故B正确;
C.S与Se位于同主族,硒化氢(H2Se)是无色、有毒气体,故C正确;
D.同主族从上到下金属增强,金属性Sr>Ba,对应最高价氧化物的水化物的碱性为氢氧化锶比氢氧化钡的碱性弱,故D错误.
故选D.
B.由卤族元素单质及化合物的递变性可知,单质的颜色随原子序数增大加深,气态氢化物稳定性减弱,则砹是一种有色固体,HAt不稳定,故B正确;
C.S与Se位于同主族,硒化氢(H2Se)是无色、有毒气体,故C正确;
D.同主族从上到下金属增强,金属性Sr>Ba,对应最高价氧化物的水化物的碱性为氢氧化锶比氢氧化钡的碱性弱,故D错误.
故选D.
点评:本题考查元素周期表的结构及应用,注意把握同主族元素性质的递变性和相似性为解答的关键,注意选项A中对角线规则,题目难度不大.

练习册系列答案
相关题目
下列不能形成配位键的组合是( )
| A、Ag+、NH3 |
| B、BF3、NH3 |
| C、Co3+、CO |
| D、NH4+、H+ |
在密闭容器中进行反应:X2(g)+3Y2(g)?2Z(g),其中X2、Y2、Z的起始浓度分别为0.1mol?L-1、0.3mol?L-1、0.2mol?L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A、c(Z)=0.5 mol?L-1 |
| B、c(Y2)=0.5 mol?L-1 |
| C、c(X2)=0.2 mol?L-1 |
| D、c(Y2)=0.6 mol?L-1 |
某芳香有机化合物,只含碳、氢、氧三种元素,且只含有一个氧原子,蒸汽的相对密度是氢气的54倍,它可能的结构共有(不考虑立体异构)( )
| A、3种 | B、4种 | C、5种 | D、6种 |
下列关于有机物的命名中不正确的是( )
| A、2-二甲基戊烷 |
| B、2-乙基戊烷 |
| C、2,3-二甲基戊烷 |
| D、3-甲基己烷 |
不能用排水集气法收集的气体是( )
| A、H2 |
| B、NO |
| C、02 |
| D、HCl |
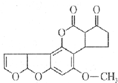 前不久,各大媒体在显著的位置刊登了关于900t致癌大米的报道,主要是变质大米中存在的黄曲霉素使人体中的特殊基因发生突变,有转变成肝癌的可能性.它的结构如图所示,和l mol该化合物起反应的H2或NaOH的最大值分别是( )
前不久,各大媒体在显著的位置刊登了关于900t致癌大米的报道,主要是变质大米中存在的黄曲霉素使人体中的特殊基因发生突变,有转变成肝癌的可能性.它的结构如图所示,和l mol该化合物起反应的H2或NaOH的最大值分别是( )| A、5mol,2mol |
| B、7mol,2mol |
| C、6mol,1mol |
| D、7mol,1mol |
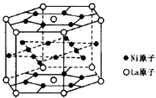 氢气是重要而洁净的能源,要利用氢气作能源,必须安全有效地储存氢气.有报道称某种合金材料有较大的储氢容量,其晶体结构的最小单元如图所示,则这种合金的化学式为( )
氢气是重要而洁净的能源,要利用氢气作能源,必须安全有效地储存氢气.有报道称某种合金材料有较大的储氢容量,其晶体结构的最小单元如图所示,则这种合金的化学式为( )| A、LaNi6 |
| B、LaNi3 |
| C、LaNi4 |
| D、LaNi5 |