��Ŀ����
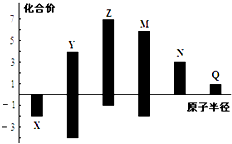
����Ŀ����ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯���������Һ����ת����ϵ����֪�ڳ��³�ѹ�£�A�ǹ��壬B��C��D��E�Ƿǽ��������Ҷ������壬C�ʻ���ɫ��������F�ǵ���ɫ���壬������G����ɫ��ӦΪ��ɫ��������I��Jͨ��״���³���̬��D��E�ķ�Ӧ�ǻ��������е�һ����Ҫ�Ĺ̵���Ӧ�� 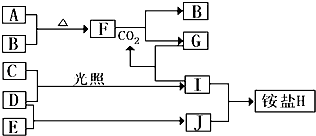
��ش��������⣺
��E ��J�ĵ���ʽ�ֱ����� ��
��д��F��CO2��Ӧ�Ļ�ѧ����ʽ���õ����ŷ���ʾ����ת�Ƶ����
�۽���������Cͨ��ʢ�е��۵⻯����Һ���Թ��У���Һ����ɫ���÷�Ӧ�����ӷ���ʽΪ ��
�ܱ����3.36L����B��A��ȫ��Ӧ��ת�Ƶ��ӵ���ĿΪ ��
���𰸡�![]() ��
�� ��
��![]() ��Cl2+2I���TI2+2Cl����1.806��1023
��Cl2+2I���TI2+2Cl����1.806��1023
���������⣺������G����ɫ��ӦΪ��ɫ������NaԪ�أ�F���������̼��Ӧ�õ����嵥��B��G������֪FΪNa2O2 �� BΪO2 �� GΪNa2CO3 �� ��A��B����������Ӧ�õ�F���������ƣ�����AΪNa��G��Na2CO3����I��Ӧ�õ�CO2 �� ��I�����ᣬI������ǽ�������C��D�ڹ��������µõ�����IΪHCl��C��D�ֱ�ΪH2��Cl2�е�һ�֣�I��Jͨ��״���³���̬�����߷�Ӧ�õ���Σ���D��E�ķ�Ӧ�ǻ��������е�һ����Ҫ�Ĺ̵���Ӧ������֪JΪNH3 �� DΪH2 �� EΪN2 �� ���ΪNH4Cl����CΪCl2 �� ��������������֪��EΪN2 �� ����ʽΪ ![]() ��JΪNH3 �� ����ʽΪ��
��JΪNH3 �� ����ʽΪ��  �����Դ��ǣ�
�����Դ��ǣ� ![]() ��
��  ����Na2O2��CO2��Ӧ�Ļ�ѧ����ʽ���õ����ŷ���ʾ����ת�Ƶ������
����Na2O2��CO2��Ӧ�Ļ�ѧ����ʽ���õ����ŷ���ʾ����ת�Ƶ������ ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ���۽���������Cl2ͨ��ʢ�е��۵⻯����Һ���Թ��У���Һ����ɫ��˵�����ɵⵥ�ʣ��÷�Ӧ�����ӷ���ʽΪ��Cl2+2I���TI2+2Cl�� �� ���Դ��ǣ�Cl2+2I���TI2+2Cl������A��B��Ӧ����ʽΪ��2Na+O2
���۽���������Cl2ͨ��ʢ�е��۵⻯����Һ���Թ��У���Һ����ɫ��˵�����ɵⵥ�ʣ��÷�Ӧ�����ӷ���ʽΪ��Cl2+2I���TI2+2Cl�� �� ���Դ��ǣ�Cl2+2I���TI2+2Cl������A��B��Ӧ����ʽΪ��2Na+O2 ![]() Na2O2 �� �μӷ�Ӧ����Ϊ
Na2O2 �� �μӷ�Ӧ����Ϊ ![]() =0.15mol����Ӧ����Ԫ����0�۽���Ϊ��1�ۣ�ת�Ƶ��ӵ���ĿΪ0.15mol��2��6.02��1023mol��1=1.806��1023 ��
=0.15mol����Ӧ����Ԫ����0�۽���Ϊ��1�ۣ�ת�Ƶ��ӵ���ĿΪ0.15mol��2��6.02��1023mol��1=1.806��1023 ��
���Դ��ǣ�1.806��1023 ��

����Ŀ��ij�о�С��Ϊ̽���������������������绯ѧ��ʴ���͵�Ӱ�����أ�����Ͼ��ȵ��������ۺ�̼��������ƿ�ײ�������ƿ��(��ͼ1)���ӽ�ͷ�ι��е��뼸�δ�����Һ��ͬʱ���������е�ѹǿ�仯��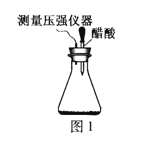
��1�����������ʵ����Ʊ�(���в�Ҫ���ո�)��
��� | ʵ��Ŀ�� | ̼��/g | ����/g | ����/% |
�� | Ϊ����ʵ�������� | 0.5 | 2.0 | 90.0 |
�� | ����Ũ�ȵ�Ӱ�� | 0.5 | ______ | 36.0 |
�� | _________ | 0.2 | 2.0 | 90.0 |
��2����Ţ�ʵ����������ѹǿ��ʱ��仯��ͼ2��t2ʱ��������ѹǿ����С����ʼѹǿ����ԭ������������______��ʴ�������ĵ缫��ӦʽΪ______������ͼ3���ü�ͷ��������ø�ʴʱ������������______����ʱ��̼�۱��淢����______(��������������ԭ��)��Ӧ��
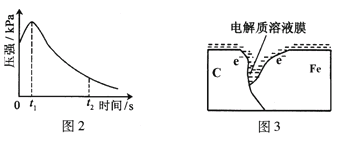
��3����С���ͼ2��0��t1ʱѹǿ����ԭ����������¼��裬������ɼ������
����һ���������ⸯʴ���������壻
�������___________________��