题目内容
|
某元素的气态氢化物的化学式为H2R,则此元素最高价氧化物对应水化物的化学式可能为 | |
A. |
H2RO3 |
B. |
H2RO4 |
C. |
HRO3 |
D. |
H3RO4 |
答案:B
解析:
解析:
|
由H2R知,R的最低负化合价为-2,则R的最高正化合价为+6,即为ⅥA族元素,其最高价氧化物对应水化物的化学式则为H2RO4. |

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
某元素的气态氢化物的化学式为XH3,其中X的质量分数约为82.4%,则X在周期表中的位置是( )
| A、第二周期VA | B、第二周期VⅡA | C、第三周期VA | D、第三周期VⅡA |
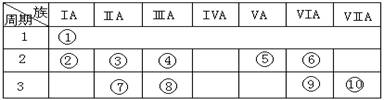
(15分)下表是元素周期表的一部分。
⑴下列说法正确且能说明元素⑩的非金属性比元素⑨强的是 。
| A.同温同压下,元素⑩的气态氢化物溶解度大于元素⑨的气态氢化物 |
| B.元素的最高价氧化物对应的水化物的酸性⑩强于⑨ |
| C.元素⑨和⑩的单质与铁反应分别得到低价、高价铁的化合物 |
| D.元素⑩的电负性大于元素⑨ |
⑶已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与盐酸反应的离子方程式:
。
⑷上述元素⑦形成的晶体对应的晶胞为下图中的___________________(填写序号)。
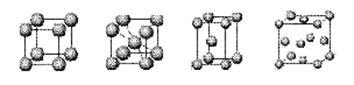
甲 乙 丙 丁
⑸元素④的含氧酸的结构式可表示为
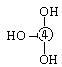 则可判断该酸为 酸(填强或弱)
则可判断该酸为 酸(填强或弱)一分子该酸与水作用,只能产生1个H+,请写出该酸溶于水后溶液显酸性的离子方程式 。
⑹已知元素⑧气态氯化物的化学式为R2Cl6,结构式如下,试并标出其中的配位键
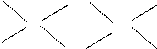 Cl Cl Cl
Cl Cl ClAl Al
Cl Cl Cl