题目内容
【题目】A,B,C,D,E为原子序数依次增大的短周期元素,已知A,B,E3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3.
(1)写出下列元素名称:A , C;
(2)比较C,D的最高价氧化物的水化物,酸性较强的是(用化学式表示).
(3)由D,E两种元素形成的化合物,其中所有原子均达到稳定结构,写出该化合物的电子式 .
(4)写出A,B两元素最高价氧化物的水化物相互反应的化学方程式: .
【答案】
(1)钠;硅
(2)H3PO4
(3)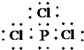
(4)Al(OH)3+NaOH═NaAlO2+2H2O
【解析】解:由“这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水”可知,在A、B、E 中必定有Al,由“A、B、C、D、E为原子序数依次增大的短周期元素”和“C元素的最外层电子数比次外层电子数少4”可知,C为Si,又由“D元素原子次外层电子数比最外层电子数多3”,所以D为P,所以只能B为Al,A为Na.E可能为Cl或S,当E为S时,不满足“A、B、E 3种原子最外层共有11个电子”,所以E只能为Cl.(1)由以上分析可知A为Na,B为Al,C为Si,D为P,E为Cl,所以答案是:钠;硅;(2)C为Si,D为P,非金属性P>Si,元素的非金属性越强,最高价氧化物的水化物的酸性越强,则H3PO4的酸性强;所以答案是:H3PO4;(3)D为P,E为Cl,PCl3中所有原子均达到稳定结构,其电子式为: ![]() ;所以答案是:
;所以答案是: ![]() ;(4)A、B两元素最高价氧化物的水化物分别为NaOH和Al(OH)3 , 相互反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O,所以答案是:Al(OH)3+NaOH═NaAlO2+2H2O.
;(4)A、B两元素最高价氧化物的水化物分别为NaOH和Al(OH)3 , 相互反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O,所以答案是:Al(OH)3+NaOH═NaAlO2+2H2O.

 阅读快车系列答案
阅读快车系列答案