题目内容
【题目】以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分Na2Cr2O7·2H2O),其主要工艺流程如下:
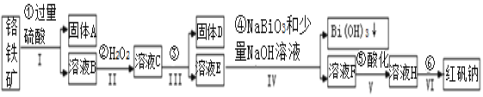
查阅资料得知:
ⅰ.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-。
ⅱ.
金属离子 | Fe3+ | Al3+ | Cr3+ | Fe2+ | Bi3+ |
开始沉淀的pH | 2.7 | 3.4 | 5.0 | 7.5 | 0.7 |
沉淀完全的pH | 3.7 | 4.9 | 5.9 | 9.7 | 4.5 |
回答下列问题:
(1)反应之前先将矿石粉碎的目的是__________________。
(2)步骤③加的试剂为_____________,此时溶液pH要调到5的目的_______________ 。
(3)写出反应④的离子反应方程式______________________。
(4)⑤中酸化是使CrO42-转化为Cr2O72-,写出该反应的离子方程式_________________。
(5)将溶液H经过蒸发浓缩,冷却结晶,过滤,洗涤,干燥即得红矾钠粗晶体,精制红矾钠则对粗晶体需要采用的操作是__________________(填操作名称)。
【答案】增大反应物的接触面积,加快反应速率,提高铬铁矿的浸取率 氢氧化钠溶液或NaOH溶液 使Fe3+、Al3+均完全转化为Fe(OH)3和Al(OH)3沉淀而除去 3NaBiO3+2Cr3++7OH-+H2O=3Bi(OH)3+2CrO42-+3Na+ CrO42-+2H+![]() Cr2O72-+H2O 重结晶
Cr2O72-+H2O 重结晶
【解析】
铬铁矿加入过量的硫酸,反应生成硫酸亚铁和硫酸铬、硫酸铝,二氧化硅不溶于硫酸,所以固体A为二氧化硅,溶液B中加入过氧化氢,将亚铁离子氧化成铁离子,加入碱调节pH使铁离子和铝离子沉淀,根据表格数据分析,控制pH到5,固体D为氢氧化铁和氢氧化铝,溶液E中加入铋酸钠和少量氢氧化钠溶液,反应生成Na2CrO4,酸化将其变成重铬酸钠,最后重结晶得到红矾钠,据此解答。
(1) 为了增大反应物的接触面积,加快反应速率,提高铬铁矿的浸取率,反应之前先将矿石粉碎,
故答案为:增大反应物的接触面积,加快反应速率,提高铬铁矿的浸取率;
(2) 根据表格数据分析,步骤③加的试剂为氢氧化钠溶液或NaOH溶液;此时溶液pH要调到5的目的使Fe3+、Al3+均完全转化为Fe(OH)3和Al(OH)3沉淀而除去,而铬离子不沉淀;
故答案为:NaOH溶液;使Fe3+、Al3+均完全转化为Fe(OH)3和Al(OH)3沉淀而除去;
(3) 反应④中铋酸钠将硫酸铬氧化生成铬酸钠同时生成氢氧化铋,离子反应方程式为 3NaBiO3+2Cr3++7OH-+H2O=3Bi(OH)3+2CrO42-+3Na+,
故答案为:3NaBiO3+2Cr3++7OH-+H2O=3Bi(OH)3+2CrO42-+3Na+;
(4) ⑤中酸化是使CrO42-转化为Cr2O72-,离子方程式2CrO42-+2H+![]() Cr2O72-+H2O,
Cr2O72-+H2O,
故答案为:2CrO42-+2H+![]() Cr2O72-+H2O;
Cr2O72-+H2O;
(5) 将溶液H经过蒸发浓缩,冷却结晶,过滤,洗涤,干燥即得红矾钠粗晶体,此操作为重结晶,
故答案为:重结晶。