题目内容
12.下列离子方程式书写正确的是( )| A. | 钠和水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 铝与稀盐酸反应:2Al+6H+═2Al3++3H2↑ | |
| C. | 铜与氯化铁溶液反应:Fe3++Cu═Fe2++Cu2+ | |
| D. | 碳酸钙与稀盐酸反应:CO32-+2H+═CO2↑+H2O |
分析 A.2mol钠与水反应生成1mol氢气,该反应不满足电子守恒;
B.铝与盐酸反应生成氯化铝和氢气;
C.离子方程式两边正电荷不相等,不满足电荷守恒;
D.碳酸钙为难溶物,离子方程式中碳酸钙不能拆开.
解答 解:A.钠和水反应生成强氧化钠和氢气,正确的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.铝与稀盐酸反应生成氯化铝和氢气,反应的离子方程式为:2Al+6H+═2Al3++3H2↑,故B正确;
C.铜与氯化铁溶液反应生成氯化亚铁和氯化铜,正确的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故C错误;
D.碳酸钙与稀盐酸反应生成氯化钙、二氧化碳气体和水,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,如:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
相关题目
2.与纯水的电离相似,液氨中也存在着微弱的电离:2NH3?NH4++NH2-,据此判断以下叙述中不正确的是( )
| A. | 液氨中含有NH3、NH4+、NH2-微粒 | |
| B. | 其他条件不变,若增加液氨的量,电离平衡将正向移动 | |
| C. | 只要不加入其他物质,液氨中c(NH4+)=c(NH2-) | |
| D. | 一定温度下液氨中c(NH4+)•c(NH2-)是一个常数 |
3.下列有关反应的颜色变化不正确的是( )
| A. | 氯水久置后黄绿色消失 | |
| B. | 淀粉溶液遇碘单质变蓝 | |
| C. | SO2使品红溶液褪色 | |
| D. | 溴水中加入CCl4溶液,振荡静置后,上层呈橙红色 |
20.下列关于硅及其氧化物的说法不正确的是( )
| A. | 硅是非金属元素,它的单质是灰黑色有金属光泽的固体 | |
| B. | 硅的导电性能介于导体和半导体之间,是良好的半导体材料 | |
| C. | 二氧化硅是酸性氧化物,不能和任何酸反应 | |
| D. | 信息高速公路的骨架----石英光导纤维的主要成份是二氧化硅 |
7.下列关于物质的性质和用途的叙述中,不正确的是( )
| A. | 硅胶吸附能力很强,常用作袋装食品、瓶装药品的干燥剂 | |
| B. | 氧化铝熔点很高,可用来制作耐火坩埚及耐高温实验仪器 | |
| C. | 二氧化硫能使品红溶液褪色,将氯气通入二氧化硫的饱和溶液中可增强其漂白性 | |
| D. | 硅导电性介于导体和绝缘体之间,是良好的半导体材料 |
17.下列物质不能由氯气与单质直接化合制得的是( )
| A. | HCl | B. | FeCl2 | C. | CuCl2 | D. | NaCl |
11.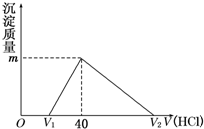 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )
 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )| A. | 原合金质量为0.92g | B. | 产生氢气0.04mol | ||
| C. | 图中m值为1.56g | D. | 图中V2为60 mL |