题目内容
【题目】N、Cu、H、O、S、Mg是常见的六种元素。
(1)Mg位于元素周期表第______周期第______族;N与O的基态原子核外未成对电子个数比为_______;Cu的基态原子电子排布式为______。
(2)用“>”或“<”填空:
碱性:Mg(OH)2______Cu(OH)2 第一电离能:O______N
熔点:MgS______MgO 稳定性:H2S______H2O
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2),Mg3N2(S)溶于足量的稀硫酸可得到两种正盐,在25℃、101kPa下,已知该反应每消耗1molH2SO4放热akJ,则该反应的热化学方程式为______。
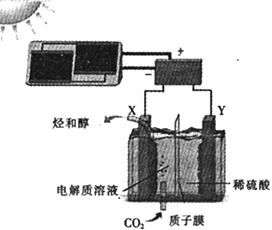
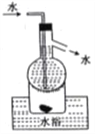
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽),写出该反应的化学方程式,并标出电子转移的方向和数目______。
【答案】三 IIA 3:2 1s22s22p63s23p63d104s1 > < < < Mg3N2(s)+4H2SO4(aq)=3MgSO4(aq)+(NH4)2SO4(aq)△H=﹣4aKJ/mol 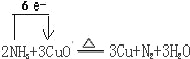
【解析】
试题 (1) 镁元素位于第三周期的IIA族。氮原子基态原子核外有3个未成对电子,氧原子有2个未成对电子,所以比例为3:2。铜为29号元素,电子排布为 [Ar]3d104s1或1s22s22p63s23p63d104s1。
(2)氢氧化镁的碱性强于氢氧化铜,氧元素和氮元素位于同一周期,从左到右,第一电离能增大。离子化合物的熔点看形成离子键的离子半径大小,硫离子半径大于阳离子,所以硫化镁的熔点小于氧化镁的熔点。非金属性越强,其气态氢化物稳定性越强,所以硫化氢的稳定性小于水。(3)氮化镁和硫酸反应生成硫酸镁和硫酸铵,所以每消耗1摩尔硫酸放热aKJ,所以消耗4摩尔硫酸,反应放热4aKJ,热化学方程式为:Mg3N2 (S) + 4 H2SO4 (aq) = 3MgSO4(aq)+ (NH4)2SO4 (aq) ΔH=-4akJ/mol。
(4)氨气和氧化铜反应生成铜和两种无污染的气体,所以生成氮气和水蒸气,方程式为:![]() 。
。

 名校课堂系列答案
名校课堂系列答案【题目】锶(Sr)与镁是同主族元素.锶的单质及其化合物用途广泛,例如金属锶用于制造合金、光电管、照明灯,Sr(OH)2用于磨拉石的提纯,Sr(NO3)2用于烟火装置,SrCl2用于修补牙齿等。
(1)锶(Sr)位于周期表的第___周期___族,过氧化锶(SrO2)中锶元素的化合价为______。
(2)金属锶在常温下和水反应,有气体生成,写出该反应的化学方程式______。
(3)金属锶很活泼,在空气中易被氧化,可保存在______中(填序号)。
①水 ②酒精 ③煤油
(4)锶的性质与钙类似。已知:CaCl2 易溶于水,CaF2难溶于水,请写出硝酸锶和氟化钠反应的离子方程式______。
(5)隔绝空气高温焙烧SrSO4和C粉的混合物,若2molSrSO4完全反应,只有S被还原并转移16mol电子,同时只生成一种可燃性气体,该反应的化学方程式:______。
(6)在t℃时,某Sr(OH)2的稀溶液中c(H+)=10—amolL—1,c(OH—)=10—bmolL—1,已知a+b=12.向该溶液中逐滴加入 pH=X 的盐酸,测得混合溶液的部分pH如表所示。
Sr(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的 pH | |
① | |||
② | 22.00 | 18.00 | 7 |
③ | 22.00 | 22.00 | 6 |
若忽略溶液混合前后的体积变化,则X为______(用数字填空)。
【题目】下列对有关微粒的相互关系和特征描述正确的是( )
选项 | 微粒 | 相互关系 | 特征描述 |
A | C60、C70、C540 | 同位素 | 微粒中只含非极性共价键 |
B | 新烷、2,2﹣二甲基丙烷 | 同分异构体 | 常温常压下呈气态 |
C |
| 同素异形体 | 铂作氨催化氧化时的催化剂 |
D | 甲酸、硬脂酸 | 同系物 | 能发生酯化反应 |
A. A B. B C. C D. D