题目内容
【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3 H2(g)![]() CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CO2(g)+ H2(g)![]() CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II
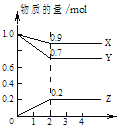
某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:

【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)![]() H2O(g) ΔH3=44.0kJ·mol-1
H2O(g) ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K= ;反应II的ΔH2= kJ·mol-1。
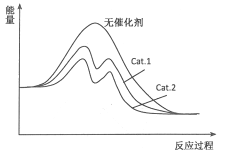
(4)在图中分别画出I在无催化剂、有Cat.1和由Cat.2三种情况下“反应过程-能量”示意图。

【答案】(1)![]() +41.2
+41.2
(4)
【解析】
试题分析:(1)根据平衡常数的公式,生成物的浓度幂之积与反应物浓度的幂之积的比值书写平衡常数为![]() 。有热化学方程式为:a:CO(g)+
。有热化学方程式为:a:CO(g)+![]() O2(g)=CO2(g) △H= -283.0kJ·mol-1 b:H2(g)+
O2(g)=CO2(g) △H= -283.0kJ·mol-1 b:H2(g)+![]() O2(g)=H2O (l)△H=-285.8kJ·mol-1 c: H2O(l)
O2(g)=H2O (l)△H=-285.8kJ·mol-1 c: H2O(l)![]() H2O(g) ΔH3=44.0kJ·mol-1根据盖斯定律分析,b-a+c即可得热化学方程式为:CO2(g)+ H2(g)
H2O(g) ΔH3=44.0kJ·mol-1根据盖斯定律分析,b-a+c即可得热化学方程式为:CO2(g)+ H2(g)![]() CO(g)+H2O(g)ΔH2=-285.8+283.0+44=+41.2 kJ·mol-1。
CO(g)+H2O(g)ΔH2=-285.8+283.0+44=+41.2 kJ·mol-1。
(4)从表中数据分析,在催化剂Cat.2的作用下,甲醇的选择性更大,说明催化剂Cat.2对反应Ⅰ的催化效果更好,催化剂能降低反应的活化能,说明使用催化剂Cat.2的反应过程中活化能更低,故图为: