题目内容
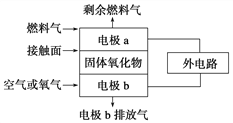
【题目】钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示。下列说法不正确的是

A. 放电时,电极A为负极,Na+由A向B移动
B. 该电池为无水电池
C. 充电时,电极B接电源的负极
D. 充电时,电极A的反应式为Na++e-=Na
【答案】C
【解析】根据图片知,放电时,Na失电子发生氧化反应,所以A作负极、B作正极,负极反应式为2Na-2e-═2Na+、正极反应式为xS+2e-═Sx2-,充电时A为阳极、B为阴极,阴极、阳极电极反应式与负极、正极反应式正好相反,放电时,电解质中阳离子向正极移动、阴离子向负极移动。A、放电时,Na失电子发生氧化反应,所以A作负极、B作正极,电解质中阳离子钠离子向正极B移动,故A错误;B、钠能够与水反应,因此电池中不能存在水,故B正确;C、充电时,B是阳极,电极B接电源的正极,故C错误;D、充电时,A是阴极,发生还原反应,电极反应式为Na++e-=Na,故D正确;故选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目