题目内容
化合物E(含两种元素)与NH3反应,生成化合物G和H2。化合物G的相对分子质量约为81,G分子中硼元素(B相对原子质量为10.8)和氢元素的质量分数分别是40%和7.4%。由此推断:
(1)化合物G的化学式为______________________________________。
(2)反应消耗1 mol NH3,可生成2 mol H2,组成化合物E的元素是___________________和_____________________。
(3)1 mol E和2 mol NH3恰好完全反应,化合物E的化学式为_______________________。
(1)化合物G的化学式为______________________________________。
(2)反应消耗1 mol NH3,可生成2 mol H2,组成化合物E的元素是___________________和_____________________。
(3)1 mol E和2 mol NH3恰好完全反应,化合物E的化学式为_______________________。
(1)N3B3H6 (2)硼(B) 氢(H) (3)B2H6
(1)n(B)=81×40%÷10.8=3
n(H)=81×7.4%÷1=6
n(N)=(81-3×10.8-6)÷14=3
所以G的分子式为N3B3H6
(2)E含两种元素,由E+NH3→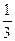 N3B3H6+2H2…①可看出E一定含硼(B)元素,另一元素也只能为H或N。由反应①式看出反应后H原子数>3,故E中一定由B、H元素构成。
N3B3H6+2H2…①可看出E一定含硼(B)元素,另一元素也只能为H或N。由反应①式看出反应后H原子数>3,故E中一定由B、H元素构成。
(3)由反应式①可知1 mol E和2 mol NH3恰好完全反应,反应式为:E+2NH3====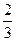 N3B3H6+4H2
N3B3H6+4H2
设E化学式为BxHy,由元素守恒得x=2
y=6,4+8-6=6,所以E化学式为B2H6。
n(H)=81×7.4%÷1=6
n(N)=(81-3×10.8-6)÷14=3
所以G的分子式为N3B3H6
(2)E含两种元素,由E+NH3→
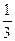 N3B3H6+2H2…①可看出E一定含硼(B)元素,另一元素也只能为H或N。由反应①式看出反应后H原子数>3,故E中一定由B、H元素构成。
N3B3H6+2H2…①可看出E一定含硼(B)元素,另一元素也只能为H或N。由反应①式看出反应后H原子数>3,故E中一定由B、H元素构成。(3)由反应式①可知1 mol E和2 mol NH3恰好完全反应,反应式为:E+2NH3====
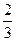 N3B3H6+4H2
N3B3H6+4H2设E化学式为BxHy,由元素守恒得x=2
y=6,4+8-6=6,所以E化学式为B2H6。

练习册系列答案
相关题目
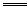 CaCO3↓+2HClO?
CaCO3↓+2HClO?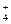 +HSO
+HSO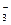 ??
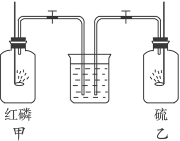
??
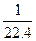
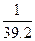 <c<
<c<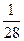
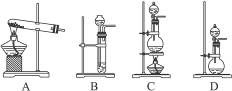
 N2+3Cu+3H2O
N2+3Cu+3H2O