题目内容
【题目】近几年来关于氮污染的治理备受关注
(1)三效催化剂是最常见的汽车尾气催化剂,能同时实现汽车尾气中的CO,CxHy,NOx三种成分的净化,其催化剂表面物质转化的关系图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定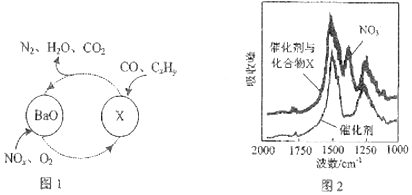
①在图示的转化中,被还原的元索是 , X的化学式为 .
②氮元素在周期表中的位置是 .
(2)SCR以技术可使NOx与NH3直接反应,实现无害转化.当NO与NO2的物质的童之比为2:l时,写出发生反应的化学方程式: . 已知NOx与NH3的反应△H<O,为提高氮氧化物的转化率可采取的措施是 . (任写一条).
(3)利用ClO2氧化氮氧化物反应过程如下:NO ![]() NO2
NO2 ![]() N2 , 反应I的化学方程式是2NO+ClO2+H2O=NO2+HNO3+2HCl,反应II的离子方程式是
N2 , 反应I的化学方程式是2NO+ClO2+H2O=NO2+HNO3+2HCl,反应II的离子方程式是
(4)加入过量次氯酸钠可使废水中NH4+完全转化为N2 , 而本身被还原为NaCl.
①写出次氯酸钠的电子式 .
②检验废水中是否存在NH4+的方法是 .
③若处理废水产生了0.448L(标准状况),则需消耗浓度为2molL﹣1的次氯酸钠的体积为 mL.
【答案】
(1)N、O;Ba(NO3)2;第二周期ⅤA族
(2)16NH3+12NO+6NO2=17N2+24H2O;降温
(3)2NO2+4SO32﹣=N2+4SO42﹣
(4)![]() ;向溶液里滴加浓NaOH溶液并加热,如果有气体放出且能使湿润的红色石蕊试纸变蓝,则溶液里含有NH4+;30
;向溶液里滴加浓NaOH溶液并加热,如果有气体放出且能使湿润的红色石蕊试纸变蓝,则溶液里含有NH4+;30
【解析】解:(1)①在图1所示的转化中N、O化合价降低为氧化剂被还原;由傅里叶红外光谱图(如图2所示)确定化合物X含硝酸根,再结合图一由钡离子参与,所以X为Ba(NO3)2;
所以答案是:N、O;Ba(NO3)2;
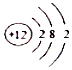
②氮元素原子的核外电子排布是2、5,所以氮元素在周期表中的位置是:第二周期ⅤA族,所以答案是:第二周期ⅤA族;(2)因为NOx与NH3的直接反应,实现无害转化,则生成氮气和水,所以当NO与NO2的物质的量之比为2:1时,发生反应的化学方程式为16NH3+12NO+6NO2=17N2+24H2O,促使化学平衡正向移动的因素就可以提高氮氧化物的转化率,反应△H<O,为提高氮氧化物的转化率可采取的措施是:降温,
所以答案是:16NH3+12NO+6NO2=17N2+24H2O;降温;(3)二氧化氮具有氧化性,亚硫酸钠具有还原性,二者之间会发生氧化还原反应:2NO2+4SO32﹣=N2+4SO42﹣ , 所以答案是:2NO2+4SO32﹣=N2+4SO42﹣;(4)①次氯酸钠为离子化合物,电子式应为 ![]() ,所以答案是:
,所以答案是: ![]() ;
;
②检验铵根离子的方法为:向待测液里加入NaOH溶液,加热,将湿润的红色石蕊试纸放在液面上方,如果溶液变蓝,则待测液中肯定含有NH4+ ,
所以答案是:向溶液里滴加浓NaOH溶液并加热,如果有气体放出且能使湿润的红色石蕊试纸变蓝,则溶液里含有NH4+ .
③因为次氯酸钠氧化废水中NH4+ 完全转化为N2 , 而本身被还原为NaCl,根据得失电子守恒,离子方程式为2NH4++3ClO﹣=N2↑+3Cl﹣+2H++3H2O,
由2NH4++3ClO﹣=N2↑+3Cl﹣+2H++3H2O得,处理废水产生了0.448L即0.02mol N2(标准状况),则需消耗浓度为2molL﹣1的次氯酸钠的体积为 ![]() ×1000ml=30ml,所以答案是:30.
×1000ml=30ml,所以答案是:30.

 考前必练系列答案
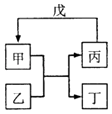
考前必练系列答案【题目】甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各物质中,不满足如图转化关系的是( )
甲 | 乙 | 丙 | 戊 | |
① | SiO2 | NaOH | Na2SiO3 | CO2 |
② | Fe | H2O | Fe2O3 | H2 |
③ | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | 过量CO2 |
④ | Na2O2 | CO2 | O2 | Na |
A.①③
B.①②
C.②④
D.①④