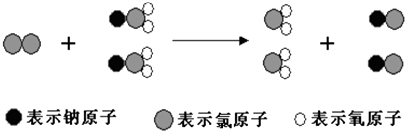
��Ŀ����
����Ŀ����һƿ��ɫ������Һ�����п��ܺ���Na+��Mg2+��Ba2+��Cl����SO ![]() ��CO
��CO ![]() ���ӣ��ֽ�������ʵ�飺 ����pH��ֽ������Һ��������Һ��ǿ���ԣ�
���ӣ��ֽ�������ʵ�飺 ����pH��ֽ������Һ��������Һ��ǿ���ԣ�
��ȡ������Һ��μ���NaOH��Һ��ʹ��Һ�����Ա�ɼ��ԣ�����������
��ȡ�������еļ�����Һ���μ�Na2CO3��Һ���а�ɫ����������
��1������������ʵȷ��������Һ�п϶����ڵ����������϶������ڵ������������ܴ��ڵ������� ��
��2��д�����з�����Ӧ�����ӷ���ʽ ��
���𰸡�
��1��Ba2+��Cl����Mg2+��SO ![]() ��CO
��CO ![]() ��Na+
��Na+
��2��Ba2++CO32��=BaCO3��
���������⣺�ɡ�������Һ�á��ã�ԭ��Һû�����Ӧ�����ӣ���ʵ��ٵ������жϣ��ų���ǿ�ᷴӦ��CO ![]() ���Ӵ��ڣ�ԭ��Һ��ǿ���ԣ����������ӿ�����Cl����SO
���Ӵ��ڣ�ԭ��Һ��ǿ���ԣ����������ӿ�����Cl����SO ![]() ��Cl����SO
��Cl����SO ![]() ����ʵ��ڵ������жϣ��ų���NaOH��Ӧ��Mg2+���ڣ�����ʵ��������жϣ�ԭ��Һ�к���Ba2+ �� ������Ba2+��Ӧ��SO
����ʵ��ڵ������жϣ��ų���NaOH��Ӧ��Mg2+���ڣ�����ʵ��������жϣ�ԭ��Һ�к���Ba2+ �� ������Ba2+��Ӧ��SO ![]() ������ԭ��Һ�д��ڵ���������Cl�� �� ͨ�������������ж�ԭ��Һ���Ƿ���Na+ �� ��1��ͨ�����Ϸ���������Һ�п϶����ڵ�������Ba2+��Cl�����϶������ڵ�������Mg2+��SO
������ԭ��Һ�д��ڵ���������Cl�� �� ͨ�������������ж�ԭ��Һ���Ƿ���Na+ �� ��1��ͨ�����Ϸ���������Һ�п϶����ڵ�������Ba2+��Cl�����϶������ڵ�������Mg2+��SO ![]() ��CO
��CO ![]() �� ���ܴ��ڵ������� Na+ �� �ʴ�Ϊ��Ba2+��Cl����Mg2+��SO
�� ���ܴ��ڵ������� Na+ �� �ʴ�Ϊ��Ba2+��Cl����Mg2+��SO ![]() ��CO
��CO ![]() �� Na+ �� ��2�����з������ӷ�Ӧ��Ba2+��CO
�� Na+ �� ��2�����з������ӷ�Ӧ��Ba2+��CO ![]() ���� BaCO3�����ķ�Ӧ���ʴ�Ϊ��Ba2++CO
���� BaCO3�����ķ�Ӧ���ʴ�Ϊ��Ba2++CO ![]() =BaCO3���� ���ݳ�����Һ�ã�ԭ��Һû�����Ӧ�����ӣ�����ʵ��������ų���ǿ�ᷴӦ�����ӣ�����ʵ��������ų���NaOH��Ӧ�����ӣ�����ʵ��������жϴ��ڵ����ӣ��ų�������ӷ�Ӧ�����ӣ�
=BaCO3���� ���ݳ�����Һ�ã�ԭ��Һû�����Ӧ�����ӣ�����ʵ��������ų���ǿ�ᷴӦ�����ӣ�����ʵ��������ų���NaOH��Ӧ�����ӣ�����ʵ��������жϴ��ڵ����ӣ��ų�������ӷ�Ӧ�����ӣ�

 ��ĩ�óɼ�ϵ�д�
��ĩ�óɼ�ϵ�д� 99��1������ĩ��ѵ��ϵ�д�
99��1������ĩ��ѵ��ϵ�д� ��ǿ��У��ĩ���100��ϵ�д�
��ǿ��У��ĩ���100��ϵ�д� �óɼ�1��1��ĩ���100��ϵ�д�
�óɼ�1��1��ĩ���100��ϵ�д� ��״Ԫ���źþ�ϵ�д�
��״Ԫ���źþ�ϵ�д�����Ŀ��д�����г��ӵ����ӷ���ʽ�������ڵ�����Ϊ���ʣ�
���ʣ����ʣ� | ���ӷ���ʽ |
FeCl2 ��FeCl3�� | ��1�� |
CO2 ��HCl�� | ��2�� |
NaHC03 ��Һ��Na2C03�� | ��3�� |
����Ŀ�������ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵķ�Ӧ����Ҫʵ��װ�����£�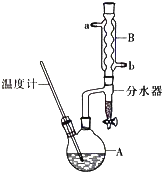
2CH3CH2CH2CH2OH ![]() ��CH3CH2CH2CH2��2O+H2O
��CH3CH2CH2CH2��2O+H2O
��Ӧ��Ͳ���������������
��Է������� | �е�/�� | �ܶ�/��gcm��3�� | ˮ���ܽ��� | |
������ | 74 | 117.2 | 0.8109 | �� |
������ | 130 | 142.0 | 0.7704 | �������� |
�ϳɷ�Ӧ��
�ٽ�6mLŨ�����37g����������һ��˳�����ӵ�A�У����Ӽ�����ʯ��
�ڼ���A�з�ӦҺ��Ѹ��������135�棬ά�ַ�Ӧһ��ʱ�䣮�����ᴿ��
�۴�A��Һ����ȴ���仺������ʢ��70mLˮ�ķ�Һ�Ҷ��У���ҡ���ã���Һ�ôֲ��
�ֲܴ���������40mLˮ��20mL NaOH��Һ��40mLˮϴ�ӣ���Һ�����Լ3g��ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ƣ�
�ݽ������������Ĵֲ�����������ռ���֣��ô���������11g��
��ش�
��1���������Ũ�����������������˳��Ϊ ��
��2������Aǰ�����ȴ� ���a����b��������B��ͨ��ˮ��
��3������۵�Ŀ���dz���ϴȥ �� ��ҡ���ã��ֲ���Ӧ�ӷ�Һ©��������ϡ����¡����ڷ������
��4������۽����һ��ˮϴ��Ŀ��Ϊ ��
��5��������У���������ʱӦ�ռ�����ѡ����ĸ�����ҵ���֣�a��100��b��117��c�� 135��d��142��
��6����Ӧ�����л�۲쵽��ˮ�����ռ���Һ�����ʣ��ҷ�Ϊ�������㣬���ŷ�Ӧ�Ľ��У���ˮ����Һ��������������ʱ���ϲ�Һ�������֧���Զ�����A����ˮ�����ϲ�Һ�����Ҫ�ɷ�Ϊ �� �²�Һ�����Ҫ�ɷ�Ϊ ��
��7����ʵ���У������ѵIJ���Ϊ ��