题目内容
11.短周期元素A、B、C、D、E的原子序数依次增大,A的一种核素的质量数为1,A和B同主族,C原子的最外层电子数是其电子层数的3倍,D的最高正价与最低负价的绝对值相等,E的最高价氧化物的水化物的化学式为HnEO2n+2.下列说法正确的是( )| A. | A+离子半径小于B+离子半径 | |
| B. | B是其所在主族元素中金属性最强的 | |
| C. | D的氧化物为酸性氧化物,溶于水可制得D的含氧酸 | |
| D. | D与E组成的化合物中,各原子最外层均达到8电子结构 |
分析 短周期元素A、B、C、D、E的原子序数依次增大,A的一种核素的质量数为1,则A为H元素;C原子的最外层电子数是其电子层数的3倍,原子只能有2个电子层,最外层电子数为6,故C为O元素;A和B同主族,B原子序数小于氧,故B为Li;D的最高正价与最低负价的绝对值相等,处于ⅣA族,故D为Si;E的最高价氧化物的水化物的化学式为HnEO2n+2,设E的最高正化合价为x,则x+n=4n+4,则x=3n+4,n只能为1,即其最高正化合价为+7,故E为Cl,据此解答.
解答 解:短周期元素A、B、C、D、E的原子序数依次增大,A的一种核素的质量数为1,则A为H元素;C原子的最外层电子数是其电子层数的3倍,原子只能有2个电子层,最外层电子数为6,故C为O元素;A和B同主族,B原子序数小于氧,故B为Li;D的最高正价与最低负价的绝对值相等,处于ⅣA族,故D为Si;E的最高价氧化物的水化物的化学式为HnEO2n+2,设E的最高正化合价为x,则x+n=4n+4,则x=3n+4,n只能为1,即其最高正化合价为+7,故E为Cl.
A.H+离子比Li+离子少一个电子层,故H+离子半径小于Li+离子半径,故A正确;
B.同主族自上而下金属性增强,同主族Li的金属性不是最强的,故B错误;
C.D的氧化物为二氧化硅,属于酸性氧化物,但二氧化硅不溶于水,也不与水反应,故C错误;
D.D与E组成的化合物为SiCl4,分子中各原子最外层均达到8电子结构,故D正确.
故选AD.
点评 本题考查位置结构性质关系综合应用,明确元素种类是解题关键,注意二氧化硅的性质,难度不大,有利于基础知识的巩固.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.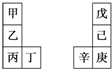 甲~辛等元素在周期表中的相对位置如表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
 甲~辛等元素在周期表中的相对位置如表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )| A. | 丙与庚的原子序数相差3 | |
| B. | 气态氢化物的热稳定性:戊>己>庚 | |
| C. | 乙所在周期元素中,其简单离子的半径最大 | |
| D. | 乙的单质在空气中燃烧生成的化合物只含离子键 |
18.下列微粒可以大量共存于同一溶液中的是( )
| A. | NH4+、CH3COO-、Ca2+、Cl- | B. | Fe3+、Ag+、SO42-、NO3- | ||
| C. | Cu2+、H+、S2-、NO3- | D. | C6H5OH、Fe3+、K+、Cl- |
15.某澄清透明溶液中,可能大量存在下列离子中的若干种:H+、NH4+、K+、Mg2+、Cu2+、Br-、AlO2-、Cl-、SO42-、CO32-,现进行如下实验:
①用试管取少量溶液,逐滴加入稀盐酸至过量,溶液先浑浊后又变澄清,有无色气体放出.将溶液分为3份.
②在第1份溶液中逐滴加入NaOH溶液至过量,溶液先浑浊后又变澄清.加热,将湿润的红色石蕊试纸置于试管口,未见明显现象.
③在第2份溶液中加入新制的氯水和CCl4,振荡后静置,下层溶液显橙红色.
则下列推断正确的是( )
①用试管取少量溶液,逐滴加入稀盐酸至过量,溶液先浑浊后又变澄清,有无色气体放出.将溶液分为3份.
②在第1份溶液中逐滴加入NaOH溶液至过量,溶液先浑浊后又变澄清.加热,将湿润的红色石蕊试纸置于试管口,未见明显现象.
③在第2份溶液中加入新制的氯水和CCl4,振荡后静置,下层溶液显橙红色.
则下列推断正确的是( )
| A. | 溶液中一定有K+、Br-、CO32-、AlO2- | |
| B. | 溶液中一定没有Mg2+、Cu2+、Cl-、NH4+ | |
| C. | 不能确定溶液中是否有K+、SO42-、Cl- | |
| D. | 往第3份溶液中滴加BaCl2可确认是否有SO42- |
16.下列物质在给定条件下同分异构体数目正确的是( )
| A. | C4H10属于烷烃的同分异构体有3种 | |
| B. | 分子组成是C5H10O2属于羧酸的同分异构体有5种 | |
| C. | 分子组成是C4H80属于醛类的同分异构体有3种 | |
| D. | 结构为 的一溴代物有5种 的一溴代物有5种 |
3.X、Y、Z、W、M均为短周期元素,X,Y同主族,X的氯化物和其最高氧化物的水化物能反应生成一种离子化合物,其水溶液显酸性;Z、W、M是第三周期连续的三种元素,其中只有一种是非金属元素,且原子半径Z>W>M.下列叙述正确的是( )
| A. | X、M两元素最简单氢化物的稳定性:X<M | |
| B. | Z、W、M的单质均能与稀硫酸反应制取氧气,且反应剧烈程度依次减弱 | |
| C. | Y的最高价含氧酸的化学式为H2YO2 | |
| D. | W和M的氧化物均可作耐高温材料 |
20.与下列事实对应的化学用语错误是( )
| A. | 纯碱溶液能清洗油污:CO32-+H2O?HCO3-+OH- | |
| B. | 配制FeSO4溶液时加入适量的铁粉:Fe3++Fe→2Fe2+ | |
| C. | 含1molNaOH和1molNa2CO3的混合溶液中滴入含1.5molHCl的稀盐酸:2OH-+CO32-+3H+→HCO3-+2H2O | |
| D. | NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42-恰好沉淀完全:2Ba2++4OH-+Al3++2SO42-→2BaSO4↓+AlO2-+2H2O |
1.如表实验所用的试剂不合理的是( )
| 选项 | 实验目的 | 所用试剂 |
| A | 比较Fe3+和Cu2+的氧化性 | FeCl3溶液和Cu |
| B | 比较镁和铝的金属性 | MgCl2溶液、AlCl3溶液、NaOH溶液 |
| C | 比较硫和氯的非金属性 | 氢硫酸、氯气 |
| D | 比较苯酚和碳酸的酸性 | 0.1mol/L苯酚钠、0.1mol/L碳酸钠溶液pH试纸 |
| A. | A | B. | B | C. | C | D. | D |
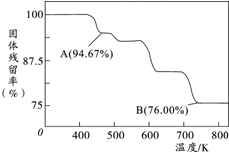 铬元素及其化合物在生产、生活中具有广泛的用途.
铬元素及其化合物在生产、生活中具有广泛的用途.