题目内容
反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45
mol,则此反应的平均速率v(X)(反应物的消耗速率或生成物的生成速率)可表示为( )
4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45
mol,则此反应的平均速率v(X)(反应物的消耗速率或生成物的生成速率)可表示为( )
A.v(NH3)=0.010 mol·(L·s)-1 B.v(O2)=0.001 mol·(L·s)-1
C.v(NO)="0.001" 0 mol·(L·s)-1 D.v(H2O)=0.045 mol·(L·s)-1
【答案】
C
【解析】
试题分析:先求出v(H2O)。由题意:
v(H2O)= ="0.001" 5 mol·(L·s)-1,D错误。再根据速率与化学计量数的关系求出v(NH3)、v(O2)、v(NO):
="0.001" 5 mol·(L·s)-1,D错误。再根据速率与化学计量数的关系求出v(NH3)、v(O2)、v(NO):
v(NH3)=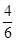 v(H2O)="0.001" 0 mol·(L·s)-1;
v(H2O)="0.001" 0 mol·(L·s)-1;
v(O2)=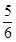 v(H2O)="0.001" 25 mol·(L·s)-1;
v(H2O)="0.001" 25 mol·(L·s)-1;
v(NO)=v(NH3)="0.001" 0 mol·(L·s)-1可见,A、B错,C对,因此正确的答案选C。
考点:考查反应速率的有关计算
点评:该题是基础性试题的考查,难度不大,主要是考查学生对反应速率概念及有关计算的熟悉了解掌握程度。常有同学不注意单位的换算而出错误;也常有同学写出左边是纯数值,而右边是“数值+单位”的不规范写法,这都是应该注意的问题。

练习册系列答案
相关题目
反应4NH3(g)+5O2(g)═4NO(g)+6H2O(g)在5L密闭容器中进行,30秒后,NO的物质的量增加了0.3mol,则此反应的平均速率v(x)(表示反应物的消耗速率或生成物的生成速率)为( )
| A、v(O2)=0.01mol?L-1?s-1 | B、v(NO)=0.002mol?L-1?min-1 | C、v(H2O)=0.003mol?L-1?s-1 | D、v(NH3)=0.001mol?L-1?s-1 |